Naujos publikacijos
Naujas metodas blokuoja vėžio ląstelių adaptaciją ir padvigubina chemoterapijos veiksmingumą
Paskutinį kartą peržiūrėta: 27.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
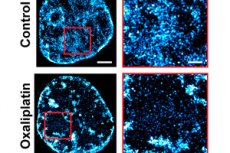
Taikydami visiškai naują vėžio gydymo metodą, Šiaurės vakarų universiteto biomedicinos inžinieriai, atlikdami eksperimentą su gyvūnais, padvigubino chemoterapijos veiksmingumą.
Užuot tiesiogiai atakavus vėžį, ši unikali strategija neleidžia vėžio ląstelėms evoliucionuoti ir tapti atsparioms gydymui, todėl liga tampa jautresnė esamiems vaistams. Šis metodas ne tik praktiškai išnaikino ligą ląstelių kultūrose, bet ir žymiai pagerino chemoterapijos veiksmingumą pelių kiaušidžių vėžio modeliuose.
Tyrimas buvo paskelbtas žurnale „ Proceedings of the National Academy of Sciences“.
„Vėžio ląstelės puikiai prisitaiko“, – sako tyrimui vadovavęs Vadimas Backmanas iš Šiaurės vakarų universiteto. „Jos gali prisitaikyti prie beveik bet ko. Pirmiausia jos išmoksta išvengti imuninės sistemos. Tada jos išmoksta atsispirti chemoterapijai, imunoterapijai ir spinduliniam gydymui. Kai jos tampa atsparios šiems gydymo būdams, jos gyvena ilgiau ir įgyja naujų mutacijų. Mes nenorėjome tiesiogiai sunaikinti vėžio ląstelių. Norėjome atimti iš jų supergalią – įgimtą gebėjimą prisitaikyti, keistis ir išvengti.“
Bekmanas yra Saksų šeimos biomedicininės inžinerijos ir medicinos profesorius Šiaurės vakarų universiteto Makkormiko inžinerijos mokykloje, kur vadovauja Fizikinės genomikos ir inžinerijos centrui. Jis taip pat yra Roberto H. Leuri visapusiško vėžio centro, Gyvybės procesų chemijos instituto ir Tarptautinio nanomokslų instituto narys.
Chromatinas yra raktas į išgyvenimą nuo vėžio
Vėžys turi daug išskirtinių bruožų, tačiau vienas bruožas slypi visuose: jo nenumaldomas gebėjimas išgyventi. Net kai imuninė sistema ir agresyvus gydymas atakuoja naviką, vėžys gali susitraukti arba sulėtinti augimą, tačiau retai kada visiškai išnyksta. Nors genetinės mutacijos prisideda prie atsparumo, mutacijos vyksta per lėtai, kad būtų galima paaiškinti greitą vėžio ląstelių reakciją į stresą.
Atlikdama seriją tyrimų, Backmano komanda atskleidė esminį mechanizmą, paaiškinantį šį gebėjimą. Sudėtinga genetinės medžiagos, vadinamos chromatinu, organizacija lemia vėžio gebėjimą prisitaikyti ir išgyventi net po stipriausių vaistų.
Chromatinas, makromolekulių grupė, apimanti DNR, RNR ir baltymus, lemia, kurie genai yra slopinami, o kurie yra ekspresuojami. Kad du metrai DNR, sudarančios genomą, tilptų vos šimtosios milimetro dalies ląstelės branduolio viduje, chromatinas yra labai suspaustas.
Derindama vaizdavimo, modeliavimo, sistemų analizės ir in vivo eksperimentų metodus, Backmano komanda nustatė, kad šio paketo 3D architektūra ne tik kontroliuoja, kurie genai yra aktyvuojami ir kaip ląstelės reaguoja į stresą, bet ir leidžia ląstelėms fiziškai užkoduoti genų transkripcijos modelių „atmintį“ į paties paketo geometriją.
Trimatis genomo išsidėstymas veikia kaip savarankiškai besimokanti sistema, panaši į mašininio mokymosi algoritmą. Jam „mokant“, šis išsidėstymas nuolat reorganizuojamas į tūkstančius nanoskopinių chromatino pakavimo domenų. Kiekviename domene saugoma ląstelės transkripcijos atminties dalis, kuri lemia, kaip ląstelė funkcionuoja.
Chromatino perprogramavimas chemoterapijai sustiprinti
Naujajame tyrime Backmanas ir jo kolegos sukūrė skaičiavimo modelį, kuris, remdamasis fizikiniais principais, analizuoja, kaip chromatino pakavimas veikia vėžio ląstelės tikimybę išgyventi chemoterapiją. Taikydama modelį skirtingų tipų vėžio ląstelėms ir chemoterapinių vaistų klasėms, komanda nustatė, kad ji gali tiksliai numatyti ląstelių išgyvenamumą – dar prieš pradedant gydymą.
Kadangi chromatino pakavimas yra labai svarbus vėžio ląstelių išgyvenimui, mokslininkai savęs paklausė: kas nutiktų, jei pakavimo architektūra būtų pakeista? Užuot kūrę naujus vaistus, jie ištyrė šimtus esamų vaistų, kad surastų kandidatus, galinčius pakeisti fizinę aplinką ląstelių branduoliuose ir paveikti chromatino pakavimą.
Galiausiai komanda pasirinko celekoksibą – FDA patvirtintą priešuždegiminį vaistą, kuris jau vartojamas artritui ir širdies bei kraujagyslių ligoms gydyti ir kuris, kaip šalutinis poveikis, keičia chromatino pakavimą.
Eksperimentiniai rezultatai
Derindami celekoksibą su standartine chemoterapija, tyrėjai pastebėjo reikšmingą žuvusių vėžio ląstelių skaičiaus padidėjimą.
Kiaušidžių vėžio pelių modeliuose paklitakselio (dažno chemoterapinio vaisto) ir celekoksibo derinys sumažino vėžio ląstelių adaptacijos greitį ir pagerino naviko augimo slopinimą, pranokdamas vien paklitakselio poveikį.
„Kai naudojome mažą chemoterapijos dozę, navikai toliau augo. Tačiau pridėjus prie chemoterapijos kandidatą TPR (transkripcijos plastiškumo reguliatorių), pastebėjome daug reikšmingesnį augimo slopinimą. Tai padvigubino veiksmingumą“, – sakė Backmanas.
Galimos perspektyvos
Ši strategija leistų gydytojams naudoti mažesnes chemoterapijos dozes, sumažinant sunkų šalutinį poveikį. Tai žymiai pagerintų pacientų komfortą ir jų patirtį gydant vėžį.
Backmanas mano, kad chromatino perprogramavimas gali būti pagrindinis veiksnys gydant kitas sudėtingas ligas, įskaitant širdies ir kraujagyslių bei neurodegeneracines ligas.
