Naujos publikacijos
Nustatytas pagrindinis baltymas, apsaugantis nuo kaulų masės mažėjimo sergant osteoporoze
Paskutinį kartą peržiūrėta: 02.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
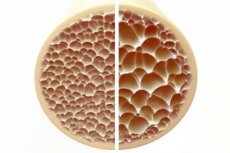
Osteoporozė, būklė, kuriai būdingi porėti ir trapūs kaulai, kelia didelę grėsmę skeleto sveikatai. Kaulai, kaip pagrindinė žmogaus kūno struktūrinė atrama, teikia gyvybiškai svarbią atramą. Kai kaulų masė mažėja, tai ne tik sutrikdo šią atramą, bet ir bendrą funkciją, todėl pablogėja gyvenimo kokybė.
Kadangi osteoporozės atvejų senstančioje populiacijoje daugėja, sveikatos priežiūros ištekliams tenka vis didesnė našta ilgalaikei priežiūrai. Todėl būtina suprasti mechanizmus, kurie prisideda prie osteoporozės vystymosi, ir sukurti veiksmingus tikslinius gydymo būdus, siekiant sumažinti ilgalaikį jos poveikį.
Osteoblastai ir osteoklastai yra dviejų tipų ląstelės, atliekančios pagrindinį vaidmenį palaikant ir pertvarkant kaulinį audinį. Osteoblastai yra kaulus formuojančios ląstelės, atsakingos už naujo kaulinio audinio sintezę ir nusėdimą, o osteoklastai yra kaulus ardančios ląstelės, dalyvaujančios seno ar pažeisto kaulinio audinio skaidyme ir pašalinime.
Osteoklastų dalies padidėjimas sukelia kaulų retėjimą tokiomis ligomis kaip osteoporozė, reumatoidinis artritas (sąnarių uždegimas) ir kaulų metastazės (vėžys, išplitęs į kaulus). Osteoklastai atsiranda diferenciuojantis makrofagams arba monocitams, kurie yra imuninių ląstelių tipas.
Taigi, osteoklastų diferenciacijos slopinimas gali būti terapinė strategija, skirta išvengti kaulų retėjimo. Tačiau tikslūs molekuliniai mechanizmai, reguliuojantys sudėtingą kaulų pertvarkymo procesą, lieka neaiškūs.
Naujame tyrime Tokijo mokslo universiteto profesorius Tadayoshi Hayata, Takuto Konno ir Hitomi Murachi kartu su kolegomis gilinosi į osteoklastų diferenciacijos molekulinį reguliavimą. Stimuliacija branduolinio faktoriaus kappa B ligando (RANKL) receptoriaus aktyvatoriumi sukelia makrofagų diferenciaciją į osteoklastus.
Be to, nustatyta, kad RANKL tarpininkaujamos osteoklastų diferenciacijos reguliavime dalyvauja kaulų morfogenetinio baltymo (BMP) ir transformuojančio augimo faktoriaus (TGF)-β signalizacijos keliai. Šiame tyrime tyrėjai siekė ištirti Ctdnep1, fosfatazės (fermento, kuris pašalina fosfatų grupes), kuri, kaip pranešama, slopina BMP ir TGF-β signalizacijos kelius, vaidmenį.
Tyrimas paskelbtas žurnale „Biocheminiai ir biofizikiniai tyrimai“.
Profesorius Hayata teigia: „RANKL veikia kaip osteoklastų diferenciacijos „greitintuvas“. Vairuojant automobilį reikia ne tik akceleratoriaus, bet ir stabdžių. Čia nustatėme, kad Ctdnep1 veikia kaip „stabdis“ osteoklastų diferenciacijos metu.“
Tyrėjai pirmiausia ištyrė Ctdnep1 ekspresiją RANKL paveiktuose pelių makrofaguose ir negydytose kontrolinėse ląstelėse. Jie pastebėjo, kad Ctdnep1 ekspresija nepakito reaguojant į RANKL stimuliaciją. Tačiau makrofaguose ji buvo lokalizuota citoplazmoje granuliuota forma ir diferencijuota į osteoklastus, skirtingai nei įprasta perinuklearinė lokalizacija kituose ląstelių tipuose, o tai rodo jos citoplazminę funkciją osteoklastų diferenciacijoje.
Be to, Ctdnep1 geno išjungimas (genų ekspresijos sumažėjęs reguliavimas) lėmė osteoklastų, teigiamų tartratui atsparios rūgšties fosfatazės (TRAP) atžvilgiu, skaičiaus padidėjimą, kur TRAP yra diferencijuotų osteoklastų žymuo.
Ctdnep1 geno išjungimas lėmė padidėjusią pagrindinių diferenciacijos žymenų, įskaitant „Nfatc1“ – pagrindinį transkripcijos faktorių, kurį RANKL indukuoja osteoklastų diferenciacijai, – raišką. Šie rezultatai patvirtina Ctdnep1 „stabdymo funkciją“, kai jis neigiamai reguliuoja osteoklastų diferenciaciją. Be to, Ctdnep1 geno išjungimas taip pat lėmė padidėjusią kalcio fosfato absorbciją, o tai rodo slopinamąjį Ctdnep1 vaidmenį kaulų rezorbcijoje.
Galiausiai, nors Ctdnep1 geno išjungimas nepakeitė BMP ir TGF-β signalizacijos, Ctdnep1 neturinčiose ląstelėse buvo padidėjęs fosforilintų (aktyvuotų) baltymų, kurie yra RANKL signalizacijos kelio produktai, kiekis. Šie rezultatai rodo, kad slopinamasis Ctdnep1 poveikis osteoklastų diferenciacijai gali būti ne perduodamas per BMP ir TGF-β signalizaciją, o per RANKL signalizacijos kelio ir Nfatc1 baltymo kiekio sumažėjimą.
Apskritai šie rezultatai suteikia naujų įžvalgų apie osteoklastų diferenciacijos procesą ir nustato galimus terapinius taikinius, kurie galėtų būti naudojami kuriant gydymo būdus, skirtus sumažinti kaulų retėjimą dėl osteoklastų hiperaktyvumo. Be ligų, kurioms būdingas kaulų retėjimas, Ctdnep1 taip pat buvo nustatytas kaip meduloblastomos, vaikų smegenų auglio, priežastinis veiksnys. Autoriai optimistiškai vertina, kad jų tyrimus galima išplėsti iki kitų žmonių ligų, neapsiribojant kaulų metabolizmu.
Profesorius Hayata daro išvadą: „Mūsų rezultatai rodo, kad Ctdnep1 yra būtinas norint išvengti pernelyg didelės osteoklastogenezės. Šie rezultatai gali dar labiau išplėsti mūsų žinias apie tai, kaip fosforilinimo-defosforilinimo tinklas kontroliuoja osteoklastų diferenciaciją, ir gali pasiūlyti naujų terapinių strategijų kaulų ligoms, susijusioms su pernelyg dideliu osteoklastų aktyvumu, gydyti.“
