Naujos publikacijos
Mokslininkai atrado naują imunosupresinį smegenų vėžio mechanizmą
Paskutinį kartą peržiūrėta: 02.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
Docentas Filippo Veglia ir jo komanda Wistar institute atrado pagrindinį mechanizmą, kuriuo glioblastoma – sunkus ir dažnai mirtinas smegenų vėžys – slopina imuninę sistemą, kad navikas galėtų augti nepaisydamas organizmo apsaugos.
Jų atradimas buvo paskelbtas žurnale „Immunity“ straipsnyje „Gliukozės sukelta histonų laktacija skatina monocitų kilmės makrofagų imunosupresinį aktyvumą glioblastomoje“.
„Mūsų tyrimas rodo, kad pakankamai gerai suprantami vėžio savaiminio įsitvirtinimo mechanizmai gali būti labai veiksmingai panaudoti kovai su liga“, – teigė dr. Veglia.
„Laukiu būsimų metabolizmo sukeltų imunosupresijos mechanizmų glioblastomos atveju tyrimų ir tikiuosi, kad toliau daugiau sužinosime apie tai, kaip geriau suprasti šį vėžį ir su juo kovoti.“
Iki šiol mažai tirta, kaip monocitų kilmės makrofagai ir mikroglijos sukuria imunosupresinę naviko mikroaplinką glioblastomoje.
„Veglia“ laboratorija tyrė glioblastomos imunosupresijos ląstelinius mechanizmus ir nustatė, kad glioblastomai progresuojant, monocitų kilmės makrofagų skaičius pradeda viršyti mikroglijos skaičių, o tai rodo, kad monocitų kilmės makrofagų dominavimas naviko mikroaplinkoje yra naudingas vėžiui, nes apsaugo nuo imuninės sistemos reakcijų.
Iš tiesų, monocitų kilmės makrofagai, bet ne mikroglijos, blokavo T ląstelių (imuninių ląstelių, kurios naikina naviko ląsteles) aktyvumą ikiklinikiniuose modeliuose ir pacientams. Komanda tai patvirtino įvertindama ikiklinikinius glioblastomos modelius su dirbtinai sumažintu monocitų kilmės makrofagų skaičiumi.
Kaip ir tikėtasi, modeliai, kuriuose naviko mikroaplinkoje buvo mažiau piktybinių makrofagų, parodė geresnius rezultatus, palyginti su standartiniais glioblastomos modeliais.
Glioblastoma sudaro kiek daugiau nei pusę visų piktybinių navikų, atsirandančių smegenyse, o pacientų, kuriems diagnozuota ši liga, prognozė yra itin prasta: tik 25 % pacientų išgyvena pirmuosius metus po diagnozės nustatymo. Glioblastoma yra pavojinga ne tik dėl savo vietos smegenyse, bet ir dėl imunosupresinės naviko mikroaplinkos, dėl kurios glioblastoma yra atspari perspektyvioms imunoterapijoms.
Programuodama tam tikras imunines ląsteles, tokias kaip makrofagai (iš monocitų gauti makrofagai ir mikroglijos), dirbti naviko labui, o ne prieš jį, glioblastoma sukuria sau naviko mikroaplinką, kuri leidžia vėžiui agresyviai augti, vengiant priešvėžinių imuninių atsakų.
Mechanizmo paaiškinimas
Patvirtinusi monocitų kilmės makrofagų vaidmenį, Weglia laboratorija siekė tiksliai suprasti, kaip šios su vėžiu susijusios imuninės ląstelės veikia prieš imuninę sistemą.
Jie sekvenavo makrofagus, kad nustatytų, ar ląstelėse yra kokių nors nenormalių genų ekspresijos modelių, kurie gali rodyti genus, kurie vaidina svarbų vaidmenį imunosupresijoje, ir taip pat ištyrė makrofagų metabolinius modelius, kad nustatytų, ar nenormali genų raiška buvo susijusi su metabolizmu.
Genų ir medžiagų apykaitos analizė juos leido nustatyti gliukozės metabolizmą. Serija bandymų parodė, kad iš monocitų gauti makrofagai, kurių gliukozės metabolizmas padidėjo ir kuriuose raiška yra pagrindinis gliukozės transporteris GLUT1, blokavo T ląstelių funkciją, išskirdami interleukiną-10 (IL-10).
Komanda įrodė, kad glioblastoma sutrikdo gliukozės metabolizmą šiuose makrofaguose, sukeldama jų imunosupresinį aktyvumą.
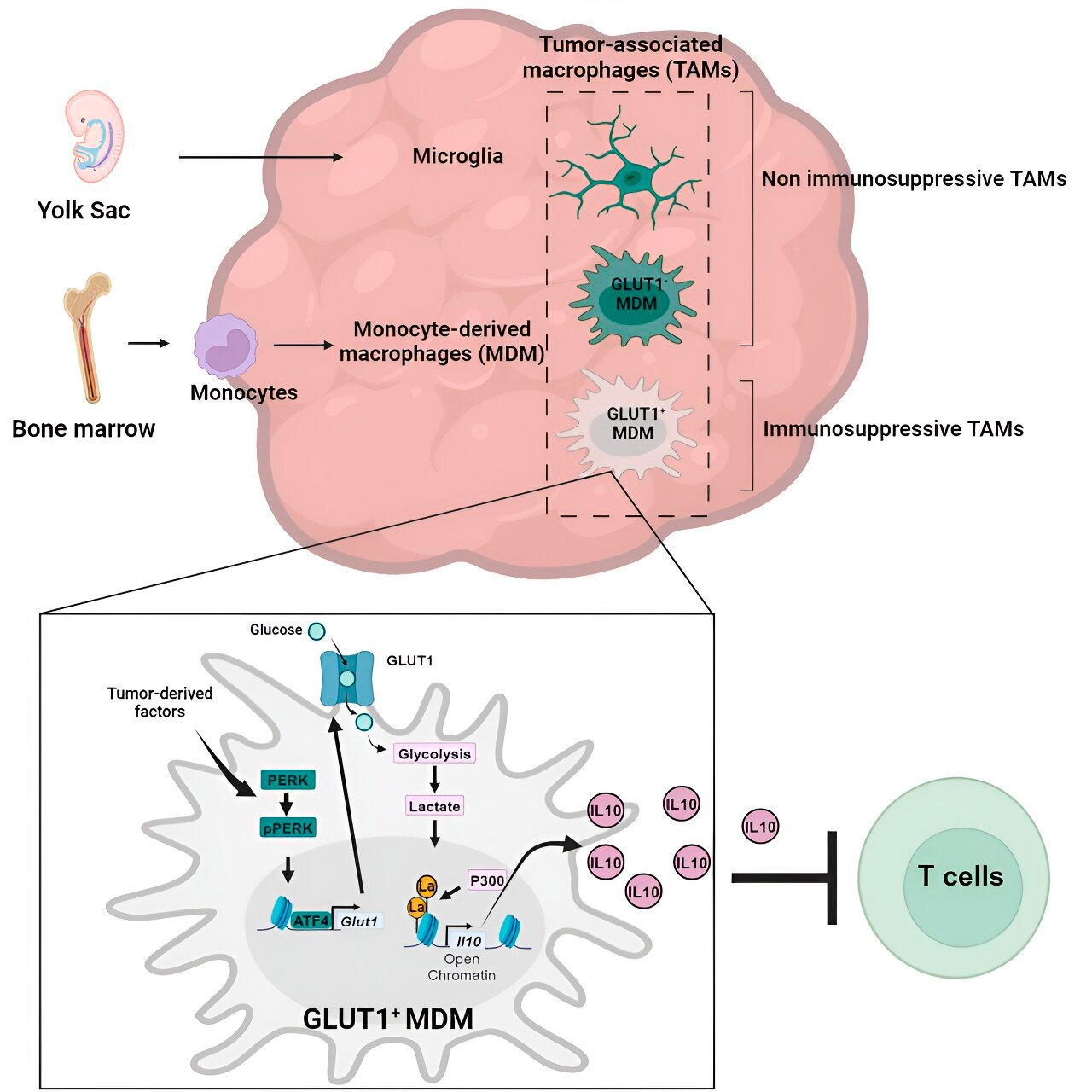
Histonų laktilinimas ir jo vaidmuo
Tyrėjai nustatė, kad monocitų kilmės makrofagų imunosupresinio aktyvumo, susijusio su gliukozės metabolizmu, raktas slypi procese, vadinamame „histono laktilinacija“. Histonai yra struktūriniai baltymai genome, kurie tam tikrais atvejais atlieka pagrindinį vaidmenį tokių genų kaip IL-10 ekspresijoje.
Greitai metabolizuodami gliukozę, monocitų kilmės makrofagai gamina laktatą – gliukozės metabolizmo šalutinį produktą. Histonai gali būti „laktilinami“ (t. y. laktatas integruojamas į histonus) taip, kad histonų organizacija skatina IL-10, kurį gamina monocitų kilmės makrofagai, siekdami palaikyti vėžio ląstelių augimą, raišką.
Problemos sprendimas
Bet kaip galima sustabdyti monocitų kilmės makrofagų imunosupresinį aktyvumą, susijusį su gliukozės metabolizmu? Dr. Veglia ir jo komanda nustatė galimą sprendimą: PERK – fermentą, kurį jie nustatė kaip gliukozės metabolizmo ir GLUT1 ekspresijos makrofaguose reguliatorių.
Ikiklinikiniuose glioblastomos modeliuose, nukreiptuose į PERK sutrikusią histonų laktilaciją ir makrofagų imunosupresinį aktyvumą, ir kartu su imunoterapija blokavo glioblastomos progresavimą ir sukėlė ilgalaikį imunitetą, kuris apsaugojo smegenis nuo naviko ataugimo, o tai rodo, kad PERK-histonų laktilacijos ašies nukreipimas gali būti perspektyvi strategija kovojant su šiuo mirtinu smegenų vėžiu.
