Medicinos ekspertas
Naujos publikacijos
Eksperimentiniai osteoartrito modeliai
Paskutinį kartą peržiūrėta: 07.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
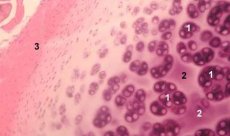
Kremzlė yra labai specializuotas audinys, sudarytas tik iš vieno tipo ląstelių (chondrocitų) ir kuriam būdingas kraujo bei limfagyslių nebuvimas. Kremzlė daugiausia maitinama absorbcija iš sinovinio skysčio. Chondrocitų metabolizmą reguliuoja daugybė tirpių veiksnių, kuriuos lokaliai gamina chondrocitai ir aplinkiniai audiniai. Chondrocitų funkcija taip pat priklauso nuo tarpląstelinės aplinkos sudėties (deguonies įtampos, jonų koncentracijos, pH ir kt.), išorinės matricos (ECM) sudėties, ląstelių ir matricos sąveikos bei fizinių signalų. Pagrindinis eksperimentinio modeliavimo tikslas – sukurti kultūras tarpląstelinėje aplinkoje, nekeičiant subrendusių ląstelių fenotipo. Antrasis tikslas – sukurti kultūras, skirtas tirti priešlaikinį, uždelstą, trumpalaikį ar užsitęsusį chondrocitų atsaką į cheminius ir (arba) fizinius signalus. In vitro tyrimai taip pat suteikia galimybę tirti chondrocitų elgesį osteoartrozės atveju. Trečiasis tikslas – sukurti bendros kultūros sistemas, leidžiančias tirti įvairių audinių sąveiką sąnaryje. Ketvirtoji užduotis – kremzlės implantų paruošimas vėlesnei transplantacijai. Galiausiai, penktoji užduotis – augimo faktorių, citokinų ar terapinių medžiagų, galinčių skatinti reparaciją ir (arba) slopinti kremzlės rezorbciją, tyrimas.
Per pastaruosius dešimtmečius buvo sukurti įvairūs sąnarinių kremzlių ląstelių kultūrų modeliai, įskaitant monosluoksnines kultūras, suspenduotas kultūras, chondronų kultūras, eksplantatus, kokultūras ir nemirtingas ląstelių kultūras. Kiekviena kultūra turi savo privalumų ir trūkumų, ir kiekviena iš jų tinka tirti vieną konkretų chondrocitų metabolizmo aspektą. Taigi, kremzlių eksplantatai yra puikus modelis tiriant matricos elementų apyvartą, kuriai reikalingi tikri ląstelių paviršiaus receptoriai ir normali ląstelių-matricos bei matricos-ląstelių sąveika. Tuo pačiu metu rekomenduojama tirti matricos sankaupas arba mechanizmus, reguliuojančius chondrocitų metabolizmą, izoliuotų ląstelių kultūroje. Mažo tankio monosluoksninė kultūra yra būtina norint tirti ląstelių diferenciacijos procesą. Natūralioje arba sintetinėje matricoje suspenduotos kultūros yra modelis, skirtas analizuoti chondrocitų adaptacinį atsaką į mechaninį stresą.
Chondrocitų kultūros
Renkantis kremzlės audinį in vitro tyrimams, reikėtų atsižvelgti į keletą svarbių dalykų. Chondrocitų matricos sudėtis ir metabolinis aktyvumas skirtinguose sąnariuose skiriasi, o pastarasis taip pat priklauso nuo chondrocitų vietos audinyje gylio. Šie duomenys buvo gauti atliekant kelis eksperimentus, kuriuose buvo tiriamos izoliuotos chondrocitų subpopuliacijos iš skirtingo gylio kremzlės zonų. Nustatyta daug morfologinių ir biocheminių skirtumų tarp kultivuotų chondrocitų, esančių paviršiniame ir giliame sąnarinės kremzlės sluoksniuose. Paviršinės ląstelės sintetina retą, proteoglikanų neturinčią fibrilinę matricą, o gilesnės ląstelės gamina matricą, kurioje gausu fibrilų ir proteoglikanų. Be to, paviršinės ląstelės gamina santykinai daugiau mažų nesuagreguotų proteoglikanų ir hialurono rūgšties bei santykinai mažiau agrekano ir keratano sulfato nei gilesni chondrocitai. Kitas svarbus chondrocitų, izoliuotų iš skirtingo gylio kremzlės zonų, metabolizmo skiriamasis bruožas yra atsakas į egzogeninį stimulą. Pasak M. Aydelotte ir kt., galvijų chondrocitai iš paviršinės kremzlės zonos buvo jautresni IL-1 nei ląstelės iš gilesnės zonos.
Ląstelių elgesys taip pat priklauso nuo audinių vietos. To paties gyvūno šonkaulių ir ausies kremzlės chondrocitai skirtingai reaguoja į augimo faktorius, tokius kaip fibroblastų augimo faktorius (FGF) ir TGF-beta. FGF padidino timidino, prolino ir leucino įsiskverbimą į kultivuojamus šonkaulių, bet ne į ausies chondrocitus. TGF-beta padidino timidino įsiskverbimą į šonkaulių ir ausies kremzlės chondrocitus, bet neturėjo įtakos timidino ir prolino įsiskverbimui į ausies chondrocitus. Kremzlės ląstelės iš didelio įtempimo sričių skiriasi nuo tų, kurios yra iš mažo kremzlės įtempimo sričių. Taigi, subrendusios avies kelio sąnario kremzlės chondrocitai iš blauzdikaulio sąnarinio paviršiaus centrinio regiono, kurio nedengia meniskas, kuris in vivo patiria didžiausią apkrovą, sintetina mažiau agrekano, bet daugiau dekorino nei ląstelės iš menisko dengtų zonų. Autoriai taip pat pabrėžia, kad tiriant sąnarių sintetinę funkciją, svarbu naudoti kremzles iš identiškų sąnarių zonų.
Chondrocitų metabolizmas ir jų reakcija į reguliavimo veiksnius taip pat labai priklauso nuo donoro amžiaus, skeleto išsivystymo ir sąnarių, iš kurių paimamos ląstelės, būklės. Žmogaus chondrocituose pastebimas reikšmingas proliferacinio atsako sumažėjimas su amžiumi. Didžiausias sumažėjimas stebimas 40–50 metų ir vyresniems nei 60 metų donorams. Be to, proliferacinio atsako į augimo faktorius (pvz., FGF ir TGF-beta) sunkumas mažėja su senėjimu. Be kiekybinių chondrocitų proliferacijos pokyčių, yra ir kokybinių pokyčių. Jaunų donorų (10–20 metų) ląstelės geriau reaguoja į trombocitų augimo faktorių (PDGF) nei į TGF-beta, o suaugusių donorų ląstelėse stebimas priešingas vaizdas. Naudojami keli mechanizmai, siekiant paaiškinti nuo amžiaus priklausomus chondrocitų sintetinės funkcijos ir jų reakcijos į augimo faktorius pokyčius. Tai apima paviršinių ląstelių receptorių skaičiaus ir afiniteto sumažėjimą, augimo faktorių ir citokinų sintezės ir bioaktyvumo pokyčius bei postreceptorinių signalų modifikaciją.
Patologinė sąnarių būklė taip pat keičia chondrocitų morfologiją ir metabolinį aktyvumą. Taigi, J. Kouri ir kt. (1996) nustatė tris chondrocitų pogrupius kremzlėje sergant osteoartritu. Paviršinės ir viršutinės kremzlės vidurio dalies chondrocitai sudaro sankaupas ir sintetina didesnį kiekį proteoglikanų ir kolageno. TGF-beta ir į insuliną panašus augimo faktorius (IGF) geba stimuliuoti proteoglikanų sintezę chondrocituose ir iš dalies neutralizuoti IL-1 ir TNF-a poveikį. Osteoartrozės pažeistos kremzlės eksplantatai ir iš osteoartroze sergančio paciento kremzlės išskirti chondrocitai yra jautresni TGF-beta stimuliacijai nei sveikos kremzlės chondrocitai. Šie skirtumai greičiausiai susiję su fenotipiniais chondrocitų pokyčiais viršutiniuose sąnarinės kremzlės sluoksniuose.
Individualūs chondrocitai išskiriami nuosekliai apdorojant ECM proteolitiniais fermentais. Išsiskyrusios iš ECM, išskirtos ląstelės idealiai tinka matrikso komponentų de novo sintezei tirti. Kai kurie autoriai naudoja tik klostridijų kolagenazę, o kiti kremzlę iš anksto inkubuoja su tripsinu, pronaze, DNaze ir (arba) hialuronidaze. Izoliuotų ląstelių skaičius priklauso nuo naudojamų fermentų. Taigi, apdorojus vien kolagenaze, iš 1 g audinio galima gauti 1,4–106 chondrocitų, o naudojant pronazę, hialuronidazę ir kolagenazę –4,3–106. Apdorojus kolagenaze, agrekanas, baltymai, IL-6 ir IL-8 ląstelių kultūroje išlieka žymiai didesniais kiekiais nei nuosekliai apdorojant skirtingais fermentais. Yra keletas šių dviejų ląstelių kultūrų skirtumų paaiškinimų:
- Ląstelių receptorius pažeidžia arba slopina fermentai, TGF-beta slopina DNR ir proteoglikanų sintezę šviežiai izoliuotuose chondrocituose (1 dieną), tuo tarpu DNR ir proteoglikanų sintezę monosluoksnyje kultivuojamuose chondrocituose (7 dienas) stimuliuoja TGF-beta. Tačiau prieš pradedant eksperimentą, reikalingas pakankamas laikotarpis šių membranos komponentų pakartotinei ekspresijai.
- Egzogeninės proteazės gali sutrikdyti integrinų sukeltą ląstelės ir matricos sąveiką. Integrinų šeima skatina chondrocitų prisijungimą prie ECM molekulių (Shakibaei M. ir kt., 1997). Šis sutrikimas gali paveikti matricos genų raišką.
- Matricos komponentų liekanos gali reguliuoti chondrocitų sintezės funkciją. Integrinai geba atpažinti ECM degradacijos produktus, todėl atlieka svarbų vaidmenį audinių atsistatyme po proteolitinių fermentų veikimo. T. Larsson ir kt. (1989) pranešė, kad į ląstelių kultūrą įdėjus sveikų arba fragmentuotų proteoglikanų, stimuliuojama baltymų ir proteoglikanų sintezė. Tačiau didelis hialurono rūgšties kiekis žymiai sumažina sulfatų įtraukimą į proteoglikanų sintezę vištos embriono chondrocituose, subrendusiuose kiaulės chondrocituose ir žiurkės chondrosarkomos ląstelėse. Be to, hialurono rūgštis slopina proteoglikanų išsiskyrimą iš ląstelių net esant IL-1b, TNF-α, FGF, o tai rodo augimo faktorių ir citokinų pirmojo biologinio aktyvumo neutralizavimą. Tikslus hialurono rūgšties veikimo mechanizmas lieka neaiškus; žinoma, kad chondrocituose yra hialurono rūgšties receptorius, susijęs su citozolio aktino filamentais. Hialurono rūgšties prisijungimas prie jos receptoriaus stimuliuoja baltymų fosforilinimą. Taigi, šie duomenys rodo, kad fragmentuotos arba natūralios matricos baltymų molekulės moduliuoja chondrocitų metabolinę funkciją, aktyvuodamos ląstelių membranų receptorius.
- Greitas chondrocitų matricos baltymų sintezės stimuliavimas fermentais gali būti chondrocitų formos pokyčių ir (arba) citoskeleto reorganizacijos pasekmė.
- Kai kurie citokinai (pvz., IL-8) ir augimo faktoriai (pvz., IGF-1, TGF-β) yra sekvestruojami ECM. Geriausiai žinomas pavyzdys yra TGF-β prisijungimas prie dekorino, dėl kurio sumažėja pirmojo gebėjimas sukelti ląstelių augimą kininių žiurkėnų kiaušidžių ląstelėse. Pastebėjimas, kad dekorino kiekis kremzlėje didėja su amžiumi, rodo, kad TGF-β biologinis prieinamumas mažėja senstant. Augimo faktoriai ir citokinai gali būti išskirti iš matricos liekanų kultūros metu ir vėliau moduliuoti chondrocitų funkciją.
Vieno sluoksnio chondrocitų kultūra
Diferencijuotas chondrocitų fenotipas pirmiausia pasižymi II tipo kolageno ir audinių specifinių proteoglikanų sinteze, taip pat mažu mitozinio aktyvumo lygiu. Yra įrodymų, kad ilgai auginant ląsteles monosluoksnyje, taip pat po kelių pakartotinių ląstelių perėjimų, chondrocitai praranda savo sferinius kontūrus ir įgauna pailgą, fibroblastų tipo formą. Esant tokiai fibroblastinei metaplazijai, pakinta ir ląstelių sintetinė funkcija, kuriai būdingas laipsniškas II, IX ir XI tipo kolageno sintezės sumažėjimas ir I, III ir Y tipo kolageno sintezės padidėjimas. Dėl funkcinio agrekano sintetinami maži neagreguoti proteoglikanai. Katepsino B ir L sintezė diferencijuotose ląstelėse yra labai maža, tačiau didėja diferenciacijos praradimo procese. Diferencijuotuose chondrocituose ekspresuojama kolagenazė-1; ilgai auginant, jos ekspresija mažėja, o audinių metaloproteazių inhibitorių (TIMP) gamyba didėja.
Diferencijuoti chondrocitai, perkelti iš monosluoksnio į suspenduotą kultūrą, pakartotinai ekspresuoja diferencijuoto fenotipo kolageną. Diferenciacijos procesas tikriausiai susijęs su ląstelės forma. Šią savybę reguliariai naudoja tyrėjai, tiriantys defektinius transplantatus su autologiniais chondrocitais. Nedidelis skaičius ląstelių, gautų iš biopsijos medžiagos, gali būti padaugintas monosluoksnio kultūroje, o po to prieš transplantaciją vėl įvestas į trimatę matricą. Dediferencijuotų chondrocitų, perkeltų į agarozės kultūrą, specifinio fenotipo pakartotinę ekspresiją gali stimuliuoti TGF-β, oseino-hidroksiapatito kompleksas ir askorbo rūgštis.
Reaguodami į augimo faktorius ir citokinus, chondrocitai diferenciacijos proceso metu yra modifikuojami. Ląstelių atsakas į citokinus ir augimo faktorius skiriasi tarp nediferencijuotų ir diferencijuotų chondrocitų. IL-1 stimuliuoja fibroblastų proliferaciją, o nediferencijuotų chondrocitų augimą slopina IL-1. DNR sintezę stimuliuoja IGF-1 pailguose, bet nesuplokštėjusiuose chondrocituose. Diferencijuotuose chondrocituose IL-1beta ir TNF-α stimuliuojantis poveikis prokolagenazės gamybai yra ryškesnis nei nediferencijuotuose chondrocituose.
Chondrocitų auginimas
Chondrocitų kultivavimas suspensijoje skystoje terpėje arba natūralioje ar sintetinėje trimatėje matricoje stabilizuoja chondrocitų fenotipą. Ląstelės išlaiko savo sferinę formą ir sintetina audiniams būdingus baltymus. Suspenduota chondrocitų kultūra paprastai rekomenduojama naujos tarpląstelinės matricos formavimosi tyrimui. Chondrocitų kultūros sintetiniuose arba natūraliuose absorbuojančiuose polimeruose naudojamos ląstelėms implantuoti į kremzlės defektus, siekiant skatinti sąnario kremzlės audinio regeneraciją. Sintetinė arba natūrali terpė implantuotoms ląstelėms turi atitikti keletą reikalavimų:
- implantai turi turėti porėtą struktūrą, kad ląstelės galėtų sukibti ir augti,
- nei pats polimeras, nei jo skaidymosi produktai implantuojant in vivo neturėtų sukelti uždegimo ar toksinių reakcijų,
- Transplantato nešiklis turi turėti galimybę prisitvirtinti prie greta esančios kremzlės arba subchondrinio kaulo,
- natūrali arba sintetinė matrica turi gebėti absorbuoti, jos skaidymą turi subalansuoti audinių regeneracija,
- Kad būtų lengviau atsistatyti kremzlei, matricos cheminė struktūra ir porų architektūra turi sudaryti sąlygas palaikyti ląstelės fenotipą ir joje esančių chondrocitų sintezę audiniams būdingiems baltymams.
- In vivo implantacijos metu būtina ištirti sintetinės arba natūralios matricos mechanines savybes.
 [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Chondrocitų suspensija skystoje fazėje
Ląstelių prisitvirtinimą prie plastikinių indų, kuriuose kultivuojami chondrocitai, galima užkirsti padengiant jų sieneles metilceliuliozės, agarozės, hidrogelio (poli-2-hidroksietilmetakrilato) arba kolageno ir agarozės mišinio tirpalu. Tokiomis sąlygomis chondrocitai sudaro grupes ir sintetina daugiausia agrekaną ir audiniams būdingus kolagenus (II, IX, XI tipų). Paprastai aptinkami dviejų tipų ląstelės. Centre esančios ląstelės išlaiko sferinę formą ir yra apsuptos gerai išsivysčiusios išorinės sienos (ECM), ką patvirtina histocheminiai ir ultrastruktūriniai tyrimai. Periferijoje chondrocitai turi disko formos kontūrus ir yra apsupti retos ECM; apie tokių ląstelių funkcines savybes mažai žinoma.
Chondrocitus galima kultivuoti ant mikronešėjų, laikomų suspensijoje; kaip mikronešėjai naudojami dekstrano granulės (citodeksas), kolagenu padengtos dekstrano granulės (citodeksas III) ir neporėtos I tipo kolageno mikrosferos (celagenas). Tokiomis kultivavimo sąlygomis chondrocitai prisitvirtina prie mikronešėjo paviršiaus, išlaiko sferinę formą ir sudaro matricos pavidalo medžiagą. Be to, celageno naudojimas skatina chondrocitų proliferaciją ir normalaus fenotipo pakartotinę raišką. Todėl chondrocitų kultivavimas ant celageno mikrosferų gali būti naudojamas ląstelių fenotipui atkurti prieš transplantaciją.
Kitas chondrocitų suspensijos kultivavimo skystoje terpėje būdas yra jų kultivavimas tankių, iš ląstelių sudarytų rutuliukų (0,5–1 * 10⁻² b ) pavidalu, gaunamų centrifuguojant. Tokie chondrocitai geba gaminti matricą, kurioje yra daug proteoglikanų, II tipo kolageno, bet ne I tipo kolageno, ką patvirtina histologiniai, imunohistocheminiai ir kiekybiniai metodai.
Chondrocitų suspensija natūraliame ECM
Chondrocitus galima kultivuoti suspensijoje trimatėje matricoje (minkštame agare, agarozėje, kolageno gelyje arba kempinėje, hialurono rūgštyje, fibrino klijuose, alginato granulėse).
Agarozėje kultivuojami chondrocitai išlaiko normalų fenotipą ir sintetina II tipo kolageną bei audiniams būdingus agrekanų agregatus. Kultivuojant agarozėje, ląstelės susintetinti proteoglikanai 50 dienų išskiriami į terpę. Palyginimui, monosluoksninėje kultūroje ląstelinė fazė perpildoma glikozaminoglikanais jau per pirmąsias 5–6 kultivavimo dienas; kultivuojant terpėje, po padidėjusios glikozaminoglikanų sintezės ir išsiskyrimo per pirmąsias 8–10 dienų, jų kiekis laikui bėgant mažėja. Nepaisant to, chondrocitų elgesys kultivuojant agarozėje skiriasi nuo elgesio in vivo. Agarozėje daugelis susintetintų agrekanų agregatų turi mažesnes molekules ir mažiau molekulių nei in vivo. TGF-β stimuliuoja proteoglikanų sintezę eksplante, bet sumažina agrekanų sintezę agarozėje.
Alginatas yra linijinis polisacharidas, gaunamas iš rudųjų jūros dumblių. Esant dvivalenčiams katijonams, tokiems kaip Ca2 + jonai, šis polimeras tampa geliu. Kiekvieną alginate įstrigusį chondrocitą supa neigiamai įkrautų polisacharidų matrica, kurios poros panašios į hialininės kremzlės poras. Alginato granulėse chondrocitų suformuota matrica susideda iš dviejų skyrių – plono su ląstelėmis susijusios matricos sluoksnio, atitinkančio sąnarinės kremzlės tarpląstelinę ir teritorinę matricą, ir tolimesnio matrikso, atitinkančio tarpląstelinę matricą natūraliame audinyje. 30-ąją kultivavimo dieną santykinis ir absoliutus ląstelių ir kiekvieno iš dviejų skyrių alginato granulėje užimamas tūris yra beveik visiškai identiškas natūralios kremzlės tūriui. Beveik 30 dienų chondrocitai išlaiko sferinę formą ir gamina agrekaną, kurio hidrodinaminės savybės panašios į sąnarinės kremzlės matricoje esančių agrekano molekulių, taip pat II, IX ir XI tipų kolageno molekules. Tuo pačiu metu, kaip ir kitose suspensijos kultūrose, alginato granulių paviršiuje yra suplokštėjusių ląstelių, kurios gamina nedidelį kiekį I tipo kolageno molekulių, kurios tiesiogiai išsiskiria į terpę ir nėra įtraukiamos į ECM. Alginato granulėse stebima vidutinė chondrocitų proliferacija. Po 8 mėnesių kultivavimo alginato gelyje subrendę chondrocitai nepraranda metabolinio aktyvumo ir toliau sintetina audiniui būdingą II tipo kolageną ir agrekaną.
H. Tanaka ir kt. (1984) tyrė įvairių natūralių molekulių difuzijos savybes alginate ir nustatė, kad didesnės nei 70 kDa molekulės nediffunduoja per alginatą. Taigi, ląstelių kultūra alginate tinka matrikso biosintezės reguliavimui ir ECM organizacijos tyrimui. Ląstelių, kultivuojamų alginate, prieinamumas leidžia tirti peptidų reguliavimo faktorių ir farmakologinių agentų poveikį transkripcijos, potranskripcijos ir transliacijos lygmenimis.
Chondrocitai taip pat kultivuojami I ir II tipų kolageno skaidulų matricoje. S. Nehrer ir kt. (1997) palygino šunų chondrocitų funkcionavimą porėtose kolageno-proteoglikano polimerinėse matricose, kuriose yra skirtingų tipų kolagenų. Jie nustatė svarbių chondrocitų, kultivuojamų kolageno matricose, kuriose yra I ir II tipų kolageno, biosintezės funkcijos morfologijos skirtumų. II tipo kolageno matricoje esančios ląstelės išlaikė savo sferinę formą, o I tipo kolageno matricoje – fibroblastų tipo morfologiją. Be to, II tipo kolageno matricoje chondrocitai gamino didesnį kiekį glikozaminoglikanų. J. van Susante ir kt. (1995) palygino alginato ir kolageno (I tipo) gelyje kultivuojamų chondrocitų savybes. Autoriai nustatė reikšmingą ląstelių skaičiaus padidėjimą kolageno gelyje, tačiau nuo 6-osios kultivavimo dienos ląstelės prarado savo būdingą fenotipą, virsdamos fibroblastų tipo ląstelėmis. Alginato gelyje pastebėtas ląstelių skaičiaus sumažėjimas, tačiau chondrocitai išlaikė normalų fenotipą. Kolageno gelyje proteoglikanų skaičius vienoje ląstelėje buvo žymiai didesnis nei alginate, tačiau gelyje nuo 6-osios kultivavimo dienos pastebėtas matricos elementų sintezės sumažėjimas, o alginate sintezė toliau didėjo.
Kieta trimatė fibrino matrica yra natūrali medžiaga, kuri palaiko diferencijuoto fenotipo joje suspenduotus chondrocitus. Trimatė fibrino matrica taip pat gali būti naudojama kaip nešiklis chondrocitų transplantacijoje. Fibrino privalumai yra citotoksiškumo nebuvimas, gebėjimas užpildyti tarpus ir adhezinė talpa. Histologiniai ir biocheminiai tyrimai, autoradiografija ir elektroninė mikroskopija parodė, kad fibrino gelyje esantys chondrocitai išlaiko savo morfologiją, proliferuoja ir gamina matricą net po 2 savaičių kultivavimo. Tačiau G. Homminga ir kt. (1993) pranešė, kad fibrino irimas prasideda po 3 dienų kultivavimo, o chondrocitų dediferenciacija progresuoja.
Chondrocitų suspensija dirbtinėje (sintetinėje) ECM terpėje
Kremzlės implantai rekonstrukcinei arba ortopedinei chirurgijai gali būti gauti auginant izoliuotus chondrocitus in vitro sintetinėje biologiškai suderinamoje matricoje.
Poliglikolio rūgštyje kultivuojami chondrocitai proliferuoja ir 8 savaites išlaiko normalią morfologiją bei fenotipą. Chondrocitų ir poliglikolio rūgšties kompleksą sudaro ląstelės, glikozaminoglikanai, kolagenai ir jis turi išorinę kolageno kapsulę. Tačiau tokiuose implantuose yra dviejų tipų kolageno molekulės – I ir II. Implantai iš chondrocitų, dediferencijuotų per eilę pasažų, turi didesnį glikozaminoglikanų ir kolageno kiekį nei implantai iš daugiausia nediferencijuotų chondrocitų.
L. Freed ir kt. (1993b) palygino žmogaus ir galvijų chondrocitų kultūrų elgseną pluoštinėje poliglikolio rūgštyje (FPGA) ir porėtoje polilaktinėje rūgštyje (PPLA). Po 6–8 savaičių galvijų chondrocitų kultivavimo FPGA arba PPLA, autoriai stebėjo ląstelių proliferaciją ir kremzlės matricos regeneraciją. FPGA chondrocitai buvo sferinės formos ir buvo išsidėstę spragose, apsuptose kremzlės matricos. Po 8 savaičių kultivavimo in vitro regeneruotame audinyje buvo iki 50 % sausosios medžiagos (4 % ląstelių masės, 15 % glikozaminoglikanų ir 31 % kolageno). PPLA ląstelės buvo verpstės formos ir turėjo nedidelį kiekį glikozaminoglikanų bei kolageno. FPGA ląstelių augimas buvo 2 kartus intensyvesnis nei PPLA. In vivo VPGK ir PPLC auginami chondrocitai per 1–6 mėnesius sukūrė audinį, histologiškai panašų į kremzlę. Implantuose buvo glikozaminoglikanų, I ir II tipo kolageno.
Galvijų vaisiaus chondrocitai buvo kultivuojami porėtame didelio tankio hidrofobiniame ir hidrofiliniame polietilene. Po 7 dienų inkubacijos abiejuose substratuose ląstelės išlaikė sferinę formą ir jose daugiausia buvo II tipo kolageno. Po 21 dienos kultivavimo nustatyta, kad hidrofilinėje matricoje yra daugiau II tipo kolageno nei hidrofobinėje matricoje.
Kremzlės audinį taip pat galima gauti kultivuojant monosluoksnyje ant „Millicell-CM“ filtrų. Chondroitinams prisitvirtinti būtina iš anksto padengti filtrus kolagenu. Histologinis kultūros tyrimas rodo chondrocitų kaupimąsi išorinėje ląstelių terpėje (ECM), kurioje yra proteoglikanų ir II tipo kolageno. I tipo kolageno tokioje kultūroje neaptikta. Gautame kremzlės audinyje esantys chondrocitai yra sferinės formos, tačiau audinio paviršiuje jie yra šiek tiek suplokštėję. Naujai susiformavusio audinio storis laikui bėgant didėjo ir priklausė nuo pradinio ląstelių monosluoksnio tankio. Optimaliomis kultivavimo sąlygomis kremzlės audinio storis pasiekė 110 μm, jo ląstelių ir kolageno organizacija į paviršinius ir gilius sluoksnius yra panaši į sąnarinės kremzlės. ECM yra maždaug 3 kartus daugiau kolageno ir proteoglikanų. Po 2 savaičių kultivavimo pastebėta matricos kaupimasis, leidžiantis audinį ištraukti iš filtro ir panaudoti transplantacijai.
Sims ir kt. (1996) tyrė chondrocitų kultivavimą polietileno oksido gelyje – kapsuliuotoje polimerinėje matricoje, kuri leidžia injekcijos būdu perkelti didelį ląstelių skaičių. Praėjus šešioms savaitėms po injekcijos į atiminių pelių poodinį audinį, susiformavo nauja kremzlė, kuri morfologiškai pasižymėjo balta opalescencija, panašia į hialininę kremzlę. Histologiniai ir biocheminiai duomenys parodė aktyviai proliferuojančių chondrocitų, gaminančių išorinę sienelę (ECM), buvimą.
Eksplantacija
Kremzlės audinio eksplantacija naudojama tiriant ana- ir katabolizmo procesus jame, homeostazės palaikymą, rezorbciją ir atstatymą. Kremzlės eksplantatuose esantys chondrocitai išlaiko normalų fenotipą ir ECM sudėtį, panašią į sąnarinėje kremzlėje in vivo. Po 5 dienų kultivavimo serume pasiekiamas pastovus sintezės lygis ir natūralūs degradacijos procesai. Audinių rezorbciją pagrindinėje kultūroje ir kultūroje, pridedant serumo, galima pagreitinti naudojant daugybę agentų, tokių kaip IL-IB, TNF-α, bakteriniai lipopolisacharidai, retinoinės rūgšties dariniai arba aktyvūs deguonies radikalai. Norint tirti kremzlės reparaciją, jos pažeidimą sukelia tirpūs uždegimo mediatoriai (H2O2 ,IL -1, TNF-α ) arba fizinis matricos plyšimas.
Organotipinės kultūros metodas yra modelis, skirtas in vitro tyrimams, kuriuose nagrinėjamas izoliuotų išorinių veiksnių poveikis chondrocitams ir juos supančiai matricai. In vivo chondrocitai yra retai išsidėstę išorinėje matricoje (ECM) ir nesiliečia vienas su kitu. Sąnarinės kremzlės eksplantato kultūra išsaugo šią struktūrinę organizaciją, taip pat specifines chondrocitų ir juos supančios tarpląstelinės aplinkos sąveikas. Šis modelis taip pat naudojamas tiriant mechaninio streso, farmakologinių medžiagų, augimo faktorių, citokinų ir hormonų poveikį kremzlės metabolizmui.
Dar vienas kremzlės audinio eksplantacijos privalumas yra tai, kad chondrocitai nepažeidžiami veikiant proteolitiniams fermentams ar mechaniniams veiksniams, o tai neišvengiama izoliuojant ląsteles. Receptoriai ir kiti membraniniai baltymai bei glikoproteinai yra apsaugoti nuo žalingų veiksnių.
 [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
[ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
Chondrono kultūra
Chondronas yra struktūrinis, funkcinis ir metabolinis sąnarinės kremzlės vienetas, susidedantis iš chondrocito, jo tarpląstelinės matricos ir kompaktiškos filamentinės kapsulės, atsakingas už matricos homeostazę. Chondronai mechaniškai išskiriami iš kremzlės ir surenkami naudojant kelis nuoseklius mažo greičio homogenizavimo procesus. Chondronus, išskirti iš skirtingo kremzlės gylio zonų, galima suskirstyti į keturias kategorijas: pavienius chondronus, porinius chondronus, kelis (tris ar daugiau) tiesiškai išdėstytus chondronus (chondronų stulpelius) ir chondronų grupes.
Pavieniai chondronai paprastai randami viduriniuose nepažeistos kremzlės sluoksniuose, poriniai chondronai – vidurinio ir giliojo sluoksnių sandūroje, tiesiškai išsidėstę daugybiniai chondronai būdingi giliesiems nepažeistos kremzlės sluoksniams. Galiausiai, chondronų sankaupos susideda iš atsitiktinai organizuotų pavienių ir porinių chondronų grupių, kurios po homogenizacijos išlaiko agregatinę būseną. Chondronų sankaupos yra dideli kremzlės fragmentai, paprastai turintys kelis chondronus ir radialiai išdėstytas kolageno fibriles, t. y. tipišką organizaciją, būdingą giliesiems matrikso sluoksniams. Chondronai imobilizuojami skaidrioje agarozėje, o tai leidžia tirti jų struktūrą, molekulinę sudėtį ir metabolinį aktyvumą. Chondronų-agarozės sistema laikoma kremzlės mikromodeliu, kuris skiriasi nuo tradicinės chondrocitų-agarozės sistemos tuo, kad išsaugoma natūrali mikroaplinka ir nereikia jos sintetinti bei surinkti. Chondronų kultūra yra modelis, skirtas tirti ląstelių ir matrikso sąveiką sąnarinėje kremzlėje normaliomis ir patologinėmis sąlygomis.
 [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
[ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
Nemirtingų chondrocitų kultūra
Rekombinantinė DNR arba onkogeną turintys virusai, galintys padaryti ląstelę „nemirtingą“, naudojami kuriant nuolatines ląstelių linijas. Nemirtingi chondrocitai turi savybę be galo daugintis, išlaikydami stabilų fenotipą. F. Mallein-Gerin ir kt. (1995) parodė, kad SV40T onkogenas sukelia pelių chondrocitų proliferaciją, kurie ir toliau stabiliai ekspresuoja II, IX ir XI tipo kolageną, taip pat sąnarinį agrekaną ir jungiamąjį baltymą. Tačiau tokia ląstelių linija įgyja gebėjimą sintetinti I tipo kolageną, kai auginama monosluoksninėje kultūroje arba agarozės gelyje.
W. Horton ir kt. (1988) aprašė nemirtingų ląstelių liniją, pasižyminčią žemu II tipo kolageno mRNR ekspresijos lygiu. Šios ląstelės buvo gautos transformuojant jas pelių retrovirusu, turinčiu I-myc- ir y-ra-onkogenus. Šis ląstelių tipas yra unikalus modelis, skirtas tirti sąnarinės matricos sąveiką nesant II tipo kolageno, taip pat II tipo kolageno sintezės reguliavimą.
Chondropritų su mutavusiais arba deletuotais genais kultūra yra patogus modelis jų fiziologinei funkcijai tirti. Šis modelis ypač tinka tiriant specifinių molekulių vaidmenį kremzlės matricos organizacijoje arba tiriant įvairių reguliavimo veiksnių poveikį kremzlės metabolizmui. Chondrocitai su deletuotu IX tipo kolageno genu sintetina platesnes nei įprastai kolageno fibriles, o tai rodo, kad IX tipo kolagenas reguliuoja fibrilių skersmenį. Kaip minėta 1 skyriuje, neseniai šeimose, sergančiose pirminiu generalizuotu osteoartritu, buvo aptikta II tipo kolageno koduojančio COLAI geno mutacija. Norėdami ištirti mutantinio II tipo kolageno poveikį sąnario matricai, R. Dharmrvaram ir kt. (1997) in vitro transfekavo (užkrėtė svetima nukleorūgštimi) defektyvų COL 2 AI (argininas 519 pozicijoje pakeistas cisteinu) į žmogaus vaisiaus chondrocitus.
Bendrakultūros sistema. Sąnaryje kremzlė sąveikauja su kitų tipų ląstelėmis, esančiomis sinovinėje membranoje, sinoviniame skystyje, raiščiuose ir subchondriniame kaule. Chondrocitų metabolizmą gali paveikti įvairūs tirpūs veiksniai, kuriuos sintezuoja išvardytos ląstelės. Taigi, sergant artritu, sąnarinę kremzlę naikina sinovinių ląstelių gaminami proteolitiniai fermentai ir laisvieji radikalai. Todėl buvo sukurti modeliai, skirti tirti sudėtingą kremzlės ir aplinkinių audinių sąveiką, kurie vadinami bendromis kultūromis.
S. Lacombe-Gleise ir kt. (1995) kultivavo triušių chondrocitus ir osteoblastus bendros kultūros sistemoje (COSTAR), kurioje ląstelės buvo atskirtos mikroporine membrana (0,4 μm), leidžiančia dviejų tipų ląstelėms keistis ląstelėmis be tiesioginio kontakto. Šis tyrimas parodė osteoblastų gebėjimą skatinti chondrocitų augimą per tirpius mediatorius.
AM Malfait ir bendraautoriai (1994) tyrė periferinio kraujo monocitų ir chondrocitų ryšį. Šis modelis yra patogus tiriant citokinų sukeltus procesus uždegiminėse artropatijose (reumatoidiniame artrite, seronegatyviuose spondiloartrituose ir kt.). Modelio autoriai atskyrė ląsteles baltymus surišančia membrana, kurios porų skersmuo buvo 0,4 μm. Tyrimas parodė, kad lipopolisacharidu stimuliuojami monocitai gamino IL-1 ir TNF-α, kurie slopino agrekano sintezę chondrocituose ir prisidėjo prie jau susintetintų agrekano agregatų skaidymo.
K. Tada ir kt. (1994) sukūrė bendros kultūros modelį, kuriame endotelio ląstelės kolageno (I tipo) gelyje buvo dedamos į vidinę kamerą, atskirtą nuo išorinės kameros, o joje – chondrocitai, patalpinti filtru, kurio porų dydis yra 0,4 μm. Visiškai izoliavus nuo išorinės kameros, žmogaus endotelio ląstelės kolageno gelyje, esant EGF arba TGF-α, suformavo vamzdelius. Kai abiejų tipų ląstelės buvo kultivuojamos vienu metu, TGF-α priklausomas vamzdelių formavimasis endotelio ląstelėse buvo slopinamas. Šio proceso slopinimą chondrocitais iš dalies panaikino anti-TGF-beta antikūnai. Galima manyti, kad chondrocitų gaminama TGF-beta slopina pačios kremzlės vaskuliarizaciją.
S. Groot ir kt. (1994) vienu metu kultivavo chondrocitus iš 16 dienų amžiaus pelės vaisiaus kaulo hipertrofinės ir proliferacinės zonų su smegenų audinio gabalėliais. Po 4 dienų kultivavimo buvo pastebėta chondrocitų transdiferenciacija į osteoblastus ir osteoidų formavimosi pradžia. Po 11 dienų kultivavimo dalis kremzlės buvo pakeista kauliniu audiniu, o kaulų matrica buvo iš dalies kalcifikuota. Kai kurie smegenų audinio gaminami neuropeptidai ir neurotransmiteriai veikia osteoblastų metabolizmą arba turi jiems receptorius. Tarp jų yra norepinefrinas, vazoaktyvus žarnyno peptidas, su kalcitonino genu susijęs peptidas, medžiaga P ir somatostatinas. Kartu su chondrocitais kultivuojami smegenų audinio gabalėliai gali gaminti kai kuriuos iš išvardytų faktorių, galinčių sukelti chondrocitų transdiferenciacijos į osteoblastus procesą.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Išorinių veiksnių įtaka chondrocitų kultūrai
Deguonies įtampos įtaka chondrocitų metabolizmui
Daugeliu atvejų chondrocitų kultūros vystosi atmosferos deguonies įtampos sąlygomis. Tačiau gerai žinoma, kad in vivo chondrocitai egzistuoja hipoksinėmis sąlygomis, o deguonies įtampa kinta esant įvairioms patologinėms sąlygoms. Brandinimo proceso metu stebimi reikšmingi epifizių kraujo tiekimo pokyčiai. Kadangi skirtingose augimo plokštelės zonose vaskuliarizacija kinta, kinta ir deguonies įtampa jose. C. Brighton ir R. Heppenstall (1971) parodė, kad triušių blauzdikaulio plokštelėje deguonies įtampa hipertrofinėje zonoje yra mažesnė nei aplinkinėje kremzlėje. Kai kurių metabolinių parametrų matavimai parodė, kad chondrocitai geba greitai reaguoti į vietinius deguonies koncentracijos pokyčius. Visų pirma, esant mažai deguonies įtampai, jo suvartojimas chondrocituose mažėja. Sumažėjus deguonies įtampai nuo 21 iki 0,04 %, padidėja gliukozės panaudojimas, padidėja glikolizės fermentų aktyvumas ir pieno rūgšties sintezė. Net ir esant mažai deguonies įtampai, absoliutus ATP, ADP ir AMP kiekis išlieka stabilus. Šie duomenys rodo, kad chondrocitų metabolizmas yra skirtas maksimaliam energijos taupymui. Tačiau sintezės aktyvumas, taigi ir reparacijos procesai, hipoksinėmis sąlygomis keičiasi.
Didelis deguonies slėgis taip pat veikia chondrocitų metabolizmą, sukeldamas proteoglikanų ir DNR sintezės sumažėjimą bei kremzlės matricos irimą. Šį poveikį paprastai lydi laisvųjų deguonies radikalų susidarymas.
Jonų koncentracijos ir aplinkos osmosinio slėgio įtaka chondrocitų funkcijai
Natūralioje kremzlėje jonų koncentracija labai skiriasi nuo koncentracijos kituose audiniuose: natrio kiekis tarpląstelinėje terpėje yra 250–350 mmol, o osmoliariškumas – 350–450 mosmol. Kai chondrocitai yra išskirti iš išorinės ląstelės (ECM) ir inkubuojami standartinėje terpėje (DMEM (Dulbecco minimali esminė terpė), osmoliariškumas yra 250–280,7 mosmol), ląsteles supanti aplinka smarkiai pasikeičia. Be to, kalcio ir kalio koncentracija standartinėje terpėje yra žymiai mažesnė nei natūraliame audinyje, o anijonų koncentracija – žymiai didesnė.
Į terpę įdėjus sacharozės, padidėja jos osmoliariškumas ir sukeliamas trumpalaikis tarpląstelinis H + ir kalcio anijonų koncentracijos padidėjimas citozolyje. Tokie tarpląsteliniai pokyčiai gali paveikti chondrocitų diferenciacijos procesus ir jų metabolinį aktyvumą. J. Urban ir kt. (1993) nustatė, kad izoliuotų chondrocitų, inkubuotų standartinėje DMEM terpėje 2–4 val., įsisavinimas 358 -sulfato ir 3H -prolino sudarė tik 10 % to, kas absorbuojama natūraliame audinyje. Sintezės intensyvumas pasiekė maksimumą, kai tarpląstelinės terpės osmoliariškumas buvo 350–400 mosmol tiek šviežiai izoliuotuose chondrocituose, tiek kremzlės audinio eksplantatuose. Be to, chondrocitų tūris padidėjo 30–40 %, įdėjus izoliuotas ląsteles į nurodyto osmoliariškumo standartinę DMEM terpę. Tačiau kultivuojant chondrocitus nefiziologinio osmoliariškumo sąlygomis 12–16 valandų, ląstelės prisitaiko prie naujų sąlygų, sumažindamos biosintezės intensyvumą proporcingai tarpląstelinės aplinkos osmoliariškumo pokyčiui.
P. Borgetti ir kt. (1995) tyrė tarpląstelinės terpės osmoliariškumo įtaką kiaulių chondrocitų augimui, morfologijai ir biosintezei. Autoriai parodė panašias biochemines ir morfologines chondrocitų, kultivuojamų terpėse, kurių osmoliariškumas yra 0,28 ir 0,38 mosmol, savybes. Esant vidutiniam 0,48 mosmol osmoliariškumui, per pirmąsias 4–6 kultivavimo valandas buvo pastebėtas ląstelių proliferacijos ir baltymų sintezės sumažėjimas, tačiau vėliau šie parametrai atsigavo ir galiausiai pasiekė kontrolines vertes. Kai chondrocitai buvo kultivuojami terpėje, kurios osmoliariškumas yra 0,58 mosmol, ląstelės prarado gebėjimą palaikyti fiziologinį proliferacinių procesų intensyvumą, o po 6 dienų chondrocitų skaičius reikšmingai sumažėjo. Esant vidutiniam 0,58 mosmol osmoliariškumui, buvo pastebėtas ryškus baltymų sintezės slopinimas. Be to, kultivuojant terpėje, kurios osmoliariškumas yra 0,28–0,38 mOsm, chondrocitai išlaiko savo fiziologinį fenotipą; Esant didesniam osmoliariškumui (0,48–0,58 mOsm), atsiranda reikšmingų ląstelių morfologijos pokyčių, kurie pasireiškia būdingo fenotipo praradimu, chondrocitų transformacija į fibroblastų tipo ląsteles ir ląstelių gebėjimo surinkti matricos proteoglikanus praradimu. Šio tyrimo rezultatai rodo chondrocitų gebėjimą reaguoti į ribotus ekstraląstelinės aplinkos osmoliariškumo svyravimus.
Kitų jonų koncentracijos pokyčiai taip pat gali turėti įtakos biosintezės procesams chondrocituose. Taigi, 35S (sulfato) įsitraukimo laipsnis padidėja perpus, padidėjus kalio jonų koncentracijai nuo 5 mmol (koncentracija standartinėje DM EM terpėje) iki 10 mmol (koncentracija ECM in vivo). Kalcio koncentracija, mažesnė nei 0,5 mmol, skatino kolageno gamybą subrendusiuose galvijų chondrocituose, o 1–2 mmol koncentracija (atitinkanti koncentraciją standartinėje DM EM terpėje) sukėlė reikšmingą kolageno sintezės sumažėjimą. Esant dideliam kalcio kiekiui (2–10 mmol), pastebėtas vidutinis biosintezės padidėjimas. Įvairūs katijonai dalyvauja chondrocitų prisijungime prie ECM baltymų. Taigi, magnio ir mangano jonai užtikrina prisijungimą prie fibronektino ir II tipo kolageno, o kalcio jonai nedalyvauja chondrocitų prisijungime prie baltymų. Taigi, aprašytų tyrimų rezultatai rodo, kad tarpląstelinių kalio, natrio, kalcio jonų ir terpės osmoliariškumo pokyčiai turi įtakos standartinėje terpėje inkubuotų chondrocitų biosintezės funkcijai.
Mechaninio streso poveikis chondrocitų metabolizmui
Sąnario imobilizacija sukelia grįžtamąją kremzlės atrofiją, kuri rodo mechaninių dirgiklių poreikį normaliems medžiagų apykaitos procesams endotelio-magistrale (EKM). Daugeliu atvejų naudojami ląstelių kultūros modeliai egzistuoja esant normaliam atmosferos slėgiui. M. Wright ir kt. (1996) parodė, kad mechaninė aplinka veikia chondrocitų metabolizmą, ląstelių atsakas priklauso nuo gniuždymo apkrovos intensyvumo ir dažnio. Eksperimentai su apkrovimu ant nepažeistų sąnarinių kremzlių eksplantų in vitro parodė baltymų ir proteoglikanų sintezės sumažėjimą veikiant statiniam apkrovimui, o dinaminis apkrovimas stimuliuoja šiuos procesus. Tikslūs mechaninio apkrovimo poveikio kremzlei mechanizmai yra sudėtingi ir tikriausiai susiję su ląstelių deformacija, hidrostatiniu slėgiu, osmosiniu slėgiu, elektriniu potencialu ir paviršiaus ląstelių receptoriais matricos molekulėms. Norint ištirti kiekvieno iš šių parametrų poveikį, būtina sukurti sistemą, kurioje vieną parametrą būtų galima keisti nepriklausomai. Pavyzdžiui, eksplantato kultūra netinka ląstelių deformacijai tirti, tačiau ji gali būti naudojama bendram slėgio poveikiui chondrocitų metaboliniam aktyvumui tirti. Kremzlės suspaudimas sukelia ląstelės deformaciją, kurią lydi hidrostatinio slėgio gradiento, elektrinio potencialo, skysčio tekėjimo atsiradimas ir tokių fizikocheminių parametrų kaip vandens kiekis matricoje, elektrinio krūvio tankis ir osmosinio slėgio lygis pokyčiai. Ląstelės deformaciją galima tirti naudojant izoliuotus chondrocitus, panardintus į agarozę arba kolageno gelį.
Sukurta keletas sistemų, skirtų mechaninio stimuliavimo poveikiui chondrocitų kultūrai tirti. Kai kurie tyrėjai naudoja sistemas, kuriose ląstelių kultūrai slėgis taikomas per dujinę fazę. Pavyzdžiui, JP Veldhuijzen ir kt. (1979), naudodami 13 kPa aukštesnį už atmosferos slėgį žemu dažniu (0,3 Hz) 15 min., pastebėjo cAMP ir proteoglikanų sintezės padidėjimą ir DNR sintezės sumažėjimą. R. Smith ir kt. (1996) parodė, kad protarpinis pirminių galvijų chondrocitų kultūros veikimas hidrostatiniu slėgiu (10 MPa) 1 Hz dažniu 4 val. sukėlė agrekano ir II tipo kolageno sintezės padidėjimą, o pastovus slėgis šiems procesams įtakos neturėjo. Naudodami panašią sistemą, Wright ir kt. (1996) pranešė, kad ciklinis slėgis ląstelių kultūrai yra susijęs su chondrocitų ląstelių membranos hiperpoliarizacija ir Ca2 + priklausomų kalio kanalų aktyvacija. Taigi, ciklinio slėgio poveikį sukelia tempimo aktyvuojami jonų kanalai chondrocitų membranoje. Chondrocitų reakcija į hidrostatinį slėgį priklauso nuo ląstelių kultūros sąlygų ir taikomo apkrovimo dažnio. Taigi, ciklinis hidrostatinis slėgis (5 MPa) sumažina sulfatų įsiskverbimą į chondrocitų monosluoksnį esant 0,05, 0,25 ir 0,5 Hz dažniui, o esant didesniam nei 0,5 Hz dažniui, sulfatų įsiskverbimas į kremzlės eksplantą padidėja.
M. Bushmann ir kt. (1992) pranešė, kad agarozės geliuose esantys chondrocitai, reaguodami į statinį ir dinaminį mechaninį krūvį, keičia biosintezę taip pat, kaip ir kultivuojamas nepažeistas organas. Autoriai nustatė, kad mechaninis krūvis sukelia hiperosmosinį stimulą, dėl kurio sumažėja chondrocitų pH.
Mechaninio tempimo poveikį galima tirti ląstelių kultūroje, panardintoje į gelį. Tempimo jėga gali būti sukurta naudojant kompiuteriu valdomą vakuumą. Kai sistema yra tam tikro laipsnio vakuume, Petri lėkštelės dugnas su ląstelių kultūra pailgėja žinomu dydžiu, deformacija yra didžiausia lėkštelės dugno kraštuose ir mažiausia centre. Tempimas taip pat perduodamas Petri lėkštelėje kultivuojamiems chondrocitams. Naudodami šį metodą, K. Holm-vall ir kt. (1995) parodė, kad chondrosarkomos ląstelėse, kultivuojamose kolageno (II tipo) gelyje, padidėja α2β integrino mRNR raiška . β2βintegrinas gali jungtis prie II tipo kolageno. Jis laikomas mechanoreceptoriumi, nes sąveikauja su aktiną surišančiais baltymais, taip sujungdamas ECM ir citoskeletą.
PH poveikis chondrocitų metabolizmui
Kremzlinio audinio ECM intersticinio skysčio pH yra rūgštesnis nei kituose audiniuose. A. Maroudas (1980) nustatė, kad sąnarinės kremzlės matricos pH yra 6,9. B. Diamant ir kt. (1966) patologinėmis sąlygomis nustatė 5,5 pH. Yra žinoma, kad chondrocitai gyvena esant mažam PO2, o tai rodo svarbų glikolizės (95 % visos gliukozės metabolizmo) vaidmenį šių ląstelių metabolizme; glikolizės metu susidaro didelis kiekis pieno rūgšties.
Be aplinkos rūgštėjimo glikolizės produktais, didelę reikšmę turi ir patys matricos komponentai. Didelis fiksuoto neigiamo krūvio kiekis proteoglikanuose keičia tarpląstelinę jonų sudėtį: stebima didelė laisvųjų katijonų (pvz., H +, Na +, K + ) ir maža anijonų (pvz., O2, HCO3) koncentracija. Be to, veikiant mechaniniam krūviui, iš išorinės ląstelės (ECM) pašalinamas vanduo, todėl padidėja fiksuotų neigiamų krūvių koncentracija ir į matricą pritraukiama daugiau katijonų. Tai lydi tarpląstelinės aplinkos pH sumažėjimas, kuris veikia tarpląstelinį pH ir taip modifikuoja chondrocitų metabolizmą. R. Wilkin ir A. Hall (1995) tyrė tarpląstelinės ir tarpląstelinės aplinkos pH įtaką matricos biosintezei, vykdomai izoliuotuose galvijų chondrocituose. Jie pastebėjo dvejopą matricos sintezės modifikaciją, sumažėjus pH. Nedidelis pH sumažėjimas (7,4 < pH < 7,1) 50 % padidino 35SO4 ir 3H-prolino įsiskverbimą į chondrocitus ,tuo tarpu gilesnis terpės parūgštinimas (pH < 7,1) 75 % slopino sintezę, palyginti su kontroline grupe. Žemo pH (6,65) sukūrimas naudojant amonio jonus lėmė matricos sintezės sumažėjimą tik 20 %. Gauti rezultatai rodo, kad matricos sintezės tarpląstelinės terpės pH modifikacijos negalima paaiškinti vien tarpląstelinės terpės pH pokyčiais. Be to, chondrocitai gali reguliuoti tarpląstelinį pH, naudodami Na +, H + mainus, Ka + priklausomą Cl_ - НСОС3 transporterį ir H + /ATPazę.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ]
Kultūrinės terpės sudėties įtaka chondrocitų metabolizmui
Chondrocitų kultivavimo terpė turi atitikti eksperimentines sąlygas. Pastaraisiais metais kultivavimo sąlygoms optimizuoti buvo naudojamas veršelio serumas. Tačiau naudojant serumą reikia atsižvelgti į keletą svarbių dalykų:
- ląstelių augimas iš audinių periferijos organų kultūrose,
- skirtingų serijų serumų sudėties kintamumas,
- nežinomų komponentų buvimas juose,
- padidėjusi interferencijos ir artefaktų rizika tiriant įvairių biologinių veiksnių įtaką ląstelių metaboliniam aktyvumui.
Pastarojo pavyzdys – EGF poveikio žiurkių kremzlės chondrocitams tyrimas. EGF stimuliavo 3H -timidino įsiskverbimą ir DNR kiekio padidėjimą kultūroje. Šis poveikis buvo ryškesnis esant mažoms serumo koncentracijoms (<1 %), tačiau esant didelėms koncentracijoms (>7,5 %) šis poveikis išnyko.
Gerai žinoma, kad DMEM terpėje, papildytoje veršelio serumu, sintezės ir skaidymo lygiai yra žymiai didesni, palyginti su sąlygomis in vivo. Skirtumai tarp metabolizmo in vivo ir in vitro gali būti susiję su sinovinio skysčio ir terpės, kurioje kultivuojamos ląstelės, skirtumais. Lee ir kt. (1997) kultivavo jaunus galvijų chondrocitus agarozėje, naudodami maistinę terpę, kurioje buvo DMEM, papildyta 20 % veršelio serumu ir dideliu kiekiu normalaus alogeninio sinovinio skysčio. Sinovinio skysčio buvimas terpėje sukėlė proteoglikanų kiekio padidėjimą iki 80 % viso sinovinio skysčio kiekio. Šie rezultatai rodo, kad sinovinis skystis kultūroje sukelia panašų metabolizmo lygį kaip ir in vivo, kai glikozaminoglikanų sintezės lygis yra aukštas, o ląstelių dalijimosi lygis – žemas.
G. Verbruggen ir kt. (1995) parodė, kad žmogaus chondrocitų, kultivuojamų agarozėje be serumo DMEM terpėje, 35S -arrpeKaHa sintezė sudarė 20–30 % sintezės lygio, stebėto DMEM terpėje, papildytoje 10 % veršelio serumo. Autoriai nustatė, kiek IGF-1, IGF-2, TGF-R arba insulinas atkūrė agrekanų gamybą terpėje be serumo. Autoriai padarė išvadą, kad 100 ng/ml insulino, IGF-1 arba IGF-2 iš dalies atkūrė agrekanų sintezę iki 39–53 % kontrolinio lygio. Nebuvo pastebėta sinergizmo ar kumuliacijos su išvardytų veiksnių deriniu. Tuo pačiu metu 10 ng/ml TGF-R, esant 100 ng/ml insulino, stimuliavo agrekanų sintezę iki 90 % ar daugiau referencinio lygio. Galiausiai, žmogaus serumo transferinas, vienas arba kartu su insulinu, neturėjo įtakos agrekanų sintezei. Kai veršelio serumas buvo pakeistas galvijų serumo albuminu, agrekanų agregatų kiekis žymiai sumažėjo. Praturtinus terpę insulinu, IGF arba TGF-R, ląstelės iš dalies atkūrė gebėjimą gaminti agrekanų agregatus. Be to, IGF-1 ir insulinas geba palaikyti homeostazę ląstelių kultūrose. Po 40 dienų kultivavimo terpėje, praturtintoje 10–20 ng/ml IGF-1, proteoglikanų sintezė išliko tokiame pačiame arba net didesnė, palyginti su terpe, kurioje buvo 20 % veršelio serumo. Kataboliniai procesai terpėje, praturtintoje IGF-1, vyko lėčiau nei terpėje, praturtintoje 0,1 % albumino tirpalu, tačiau šiek tiek greičiau terpėje, praturtintoje 20 % serumo. Ilgaamžėse kultūrose 20 ng/ml IGF-1 palaiko stabilią ląstelių būseną.
D. Lee ir kt. (1993) palygino kultūros terpės sudėties (DMEM, DMEM+20 % veršelio serumo, DMEM+20 ng/ml IGF-1) poveikį DNR sintezei kremzlės audinio eksplanto kultūroje, monosluoksninėje kultūroje ir agarozės suspensijoje. Kultivuojant agarozėje su serumu, autoriai pastebėjo chondrocitų tendenciją grupuotis į dideles grupes. Ląstelės, kultivuojamos be serumo arba su IGF-1, agarozėje išlaikė apvalią formą, buvo surinktos į mažas grupes, bet nesudarė didelių agregatų. Monosluoksnyje DNR sintezė buvo žymiai didesnė terpėje su serumu nei terpėje, praturtintoje IGF-1; pastarojoje DNR sintezė buvo žymiai didesnė nei nepraturtintoje terpėje. Chondrocitus kultivuojant agarozės suspensijoje nepraturtintoje terpėje ir terpėje su IGF-1, DNR sintezės skirtumų nerasta. Tuo pačiu metu, kultivuojant chondrocitų suspensijas agarozėje serumu praturtintoje terpėje, palyginti su kitomis terpėmis, padidėjo radionukleotido 3H-timidino įterpimas .
Vitaminas C yra būtinas fermentų, dalyvaujančių stabilios spiralinės kolageno fibrilų struktūros formavime, aktyvavimui. Askorbo rūgšties stokojantys chondrocitai sintetina nepakankamai hidroksilintus nespiralinius kolageno pirmtakus, kurie lėtai sekretuojami. Askorbo rūgšties (50 μg/ml) vartojimas sukelia II ir IX tipo kolageno hidroksilinimą ir jų sekreciją normaliu kiekiu. Vitamino C pridėjimas neturėjo įtakos proteoglikanų sintezės lygiui. Todėl kolageno sekrecija reguliuojama nepriklausomai nuo proteoglikanų sekrecijos.

