Medicinos ekspertas
Naujos publikacijos
Prostatos vėžio stadijų diagnostika
Paskutinį kartą peržiūrėta: 04.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
Kliniškai skiriamas lokalizuotas (T1-2 , N0 , M0 ), lokaliai išplitęs (T3-4 , N0-1 , M0 ) ir generalizuotas vėžys (T1-4 , N0-1 , M1 ).
Pacientai, kuriems yra kliniškai lokalizuota ir lokaliai išplitusi stadija, klasifikuojami pagal rizikos laipsnį (D'Amico A V. ir kt., 2003):
- žemas: T1a -c stadija; PSA lygis mažesnis nei 10 ig/ml: Gleason įvertinimas – 2–5; biopsijoje – vienpusis pažeidimas mažesnis nei 50 %:
- vidutinio sunkumo: T2a stadija; PSA lygis mažesnis nei 10 ng/ml; Gleason skalė - 3 + 4 = 7; biopsijoje - abipusis pažeidimas mažesnis nei 50%;
- aukšta stadija T2b , T3a -b; PSA lygis - 10-20 ng/ml; Gleason įvertinimas - daugiau nei 4 + 3 - 7; biopsijoje - pažeidimas didesnis nei 50%, tarpvietės invazija;
- labai aukšta: T4 stadija ; PSA lygis didesnis nei 20 ng/ml; Gleasono skalė didesnė nei 8; biopsijoje matoma limfovaskulinė invazija.
Patikslinus diagnozę ir nustačius proceso mastą (lokalizuotas, lokaliai išplitęs ar generalizuotas), gydytojas ir pacientas susiduria su gydymo metodo pasirinkimu. Šiuolaikinėje visuomenėje didelė reikšmė teikiama pacientų gyvenimo kokybei pradėjus gydymą. Gyvenimo kokybė be gydymo atitinka pagrindinės ligos eigą ir priklauso nuo onkologinio proceso progresavimo. Gyvenimo kokybės pokyčiai daugiausia vyksta pradėjus gydymą ir pritaikius vieną iš terapinių ar chirurginių metodų. Aiškiai nustatant proceso stadiją, galima ne tik pasirinkti optimalų gydymo metodą, bet ir numatyti tolesnę ligos eigą.
PSA lygio nustatymas kartu su klinikiniu prostatos vėžio vaizdu ir naviko gradacija pagal Gleasono skalę žymiai padidina kiekvieno iš išvardytų rodiklių informacinį turinį nustatant patologinę vėžio stadiją. AV Partin ir kt. (1997) pasiūlė prognostines lenteles, leidžiančias numatyti tolesnį naviko plitimą, gydymo metodo pasirinkimą, radikalumo laipsnį ir gydymo efektyvumo prognozę.
Naviko išplitimui įvertinti dažniausiai naudojami metodai yra DRE, TRUS, PSA lygio nustatymas ir kaulų scintigrafija. Prireikus skiriama kompiuterinė tomografija (KT) arba magnetinio rezonanso tomografija (MRT) ir krūtinės ląstos rentgenograma.
Bet kuris iš vaizdinimo metodų skirtas nustatyti stadiją ir įvertinti gydymo veiksmingumą. Patvirtinęs diagnozę, urologas turi išsiaiškinti pirminio naviko tūrį, jo ribas, naviko invazinį ar metastazinį potencialą. Visi šie rodikliai yra labai svarbūs ligos prognozei ir gydymo metodo pasirinkimui.
Pirminis navikas (T)
Pirmiausia reikia nustatyti, ar navikas apsiriboja prostata (T1-2 ), ar išeina už kapsulės ribų (T3-4 ). Skaitmeninis tyrimas dažnai neleidžia įvertinti naviko išplitimo. Kai kuriais duomenimis, mažiau nei 50 % pacientų DRE rezultatai atitinka histologinio tyrimo rezultatus. Tačiau išsamesnis tyrimas indikuotinas tik sprendžiant dėl radikalaus gydymo.
PSA lygis gali atspindėti naviko išplitimą, tačiau neleis tiksliai nustatyti morfologinės stadijos. PSA lygio, Glisono indekso ir palpacijos duomenų derinys leidžia geriau numatyti morfologinę stadiją nei kiekvienas iš šių parametrų atskirai. Laisvojo PSA vertė kelia ginčų: vieno tyrimo metu laisvojo PSA kiekio nustatymas padėjo patikslinti lokalizuotų navikų stadiją, tačiau kiti tyrimai to nepatvirtino. Tik išsamūs tyrimai padės išspręsti šią problemą.
Dažniausiai prostatos liaukos būklei ištirti naudojamas transrektalinis ultragarsas. Šiuo metodu galima aptikti tik 60 % navikų ir ne visada parodo kapsulės invaziją. Beveik 60 % pacientų, sergančių T3 stadija . Ultragarsas rodo retesnį procesą. Ultragarsiniai kapsulės invazijos požymiai yra liaukos kontūro išsipūtimas, nelygumas ir plyšimas. Naviko ląstelių invazija į sėklines pūsleles yra blogas prognostinis požymis, tačiau informacija apie jį yra labai svarbi renkantis gydymo metodą. Atliekant TRUS, reikia atkreipti dėmesį į pūslelių echostruktūrą (hiperechogeniškumą), jų asimetriją, deformaciją ir išsiplėtimą. Taip pat sėklinių pūslelių pažeidimą rodo apvalumo praradimas ir sutankinimas liaukos apačioje. Šie požymiai yra gana subjektyvūs, todėl netikslinga visiškai pasikliauti ultragarso duomenimis. Sėklinių pūslelių invazija rodo didelę vietinio recidyvo ir metastazių riziką, o jų biopsija nurodoma patikslinimui (prieš operaciją). Tyrimo nereikėtų pradėti šia procedūra, tačiau jei invazijos rizika yra didelė ir gydymo pasirinkimas priklauso nuo biopsijos rezultato, jos taikymas yra pagrįstas. Neigiamas rezultatas neatmeta mikroskopinės invazijos. Paprastai sėklinių pūslelių biopsija atliekama esant T2b ir aukštesnei klinikinei stadijai, o PSA kiekis yra didesnis nei 10 ng/ml. Rezultatas laikomas teigiamu, jei bent vienoje biopsijoje iš prostatos pamato yra naviko ląstelių. Ne tik papildomi tyrimai, bet ir išsami pirminės biopsijos rezultatų analizė leidžia padidinti klinikinio stadijos nustatymo tikslumą (tampa naviko židinių skaičius ir mastas, kapsulės invazija). Taip pat svarbus diferenciacijos laipsnis: kai Gleasono indeksas yra mažesnis nei 6, navikas lokalizuojasi 70 % atvejų.
Kraujo tekėjimas prostatos liaukoje, sergant vėžiu, yra didesnis nei normalioje liaukoje arba esant jos hiperplazijai. Po kastracijos kraujo tekėjimo intensyvumas liaukoje sumažėja. Echoskopinių žemėlapių, skirtų prostatos vėžio diagnostikai ir stebėjimui, kūrimas yra perspektyvus, tačiau šiuo metu nėra patikimų duomenų apie echoskopinės diagnostikos taikymą nustatant vietinio proceso stadiją. Šiuo metodu galima gauti papildomos medžiagos tikslinės biopsijos metu iš patologinės vaskuliarizacijos židinių.
Prostatos vėžio vizualizacijos rezultatai tiesiogiai priklauso nuo klinikos techninės įrangos ir specialisto patirties. Štai kodėl visi šiuolaikiniai vizualizacijos metodai atlieka ne lemiamą, o aiškinamąjį vaidmenį, o gydymo metodo pasirinkimas grindžiamas klinikinių tyrimų duomenų ir instrumentinių tyrimų deriniu.
MRT turi geriausias galimybes vizualizuoti prostatos struktūrą. Šiuolaikinis dubens organų tyrimo standartas naudojant MRT metodą yra endorektalinio jutiklio naudojimas, leidžiantis gauti vaizdą su didžiausia įmanoma 0,5–1 mm erdvine skiriamąja geba. Į endorektalinį jutiklį įpučiant oro, aiškiai matoma prostatos kapsulė, tiesiosios prostatos kampai ir Denonvillierio tiesiosios prostatos fascija. Endorektalinio jutiklio naudojimas MRT neriboja regioninių limfmazgių vizualizavimo (iki pilvo aortos bifurkacijos lygio). Prostatos vėžiui būdingas mažas signalo intensyvumas T svertiniuose vaizduose, kai fone yra didelis signalas iš nepakitusios liaukos periferinės zonos. Netaisyklinga forma, difuzinis išplitimas su masės efektu, neryškūs ir nelygūs kontūrai yra morfologinės mažo signalo intensyvumo židinių prostatos periferinėje zonoje charakteristikos, rodančios pažeidimo neoplastinį pobūdį. Atliekant dinaminį kontrastavimą, vėžio židiniai greitai kaupia kontrastinę medžiagą arterinėje fazėje ir greitai ją pašalina, o tai atspindi angiogenezės laipsnį ir atitinkamai naviko piktybiškumo laipsnį. Mažas signalo intensyvumas taip pat būdingas po biopsijos atsiradusių kraujavimų židiniams, prostatitui, gerybinei stromos liaukos neutralios zonos hiperplazijai, fibroziniams-randiniams pokyčiams, fibromuskulinei hiperplazijai, hormoninės ar spindulinės terapijos pasekmėms. MRT be dinaminio kontrastavimo neleidžia patikimai diferencijuoti daugumos išvardytų pokyčių ir ligų.
Kaip minėta pirmiau, vienas iš pagrindinių bet kurio prostatos vėžio vaizdinimo metodo uždavinių yra nustatyti liaukos pažeidimo tūrį ir naviko išplitimą už kapsulės ribų. Naviko tūrio nustatymas yra svarbus prognozei. Naviko tūris, mažesnis nei 4 cm3, rodo tolimas metastazes, o 12 cm3 – itin didelę metastazių tikimybę. Tyrimų duomenimis, MRT tikslumas nustatant prostatos liaukos navikinių pažeidimų židinius svyruoja nuo 50 iki 90%. MRT jautrumas nustatant prostatos vėžio lokalizaciją yra apie 70–80%, o mikroskopinių vėžio židinių (židinių) MRT pagalba aptikti neįmanoma.
Svarbiausias endorektalinio MRT privalumas yra galimybė lokalizuoti navikinius pažeidimus tose vietose, kurios nepasiekiamos kitais diagnostiniais metodais, ir išsiaiškinti naviko augimo pobūdį bei kryptį. Pavyzdžiui, MRT leidžia aptikti navikinius pažeidimus prostatos periferinės zonos priekinėse dalyse, kurios nepasiekiamos atliekant transrektalinę biopsiją. Apskritai MRT reikšmingai papildo DRE ir TRUS duomenis apie naviko lokalizaciją.
Endorektalinis MRT leidžia vizualizuoti liaukos kapsulę, kraujagyslių-nervų pluoštus, sėklines pūsleles, liaukos viršūnę, periprostatinį veninį rezginį ir nustatyti vietinį liaukos naviko paplitimą. Reikėtų pabrėžti, kad kapsulės prasiskverbimas laikomas mikroskopiniu požymiu, ir net šiuolaikiniai MRT prietaisai (endorektalinė spiralė) negali pateikti tokios informacijos. Galima gauti duomenis tik apie augimą už liaukos kapsulės ribų.
Ekstrakapsulinio išplitimo diagnostiniai kriterijai naudojant MRT:
- ekstrakapsulinio naviko buvimas;
- netolygus liaukos kontūras (deformacija, kampuotumas);
- neurovaskulinių ryšulių asimetrija;
- tiesiosios prostatos kampų obliteracija;
- platus naviko kontaktas su kapsule.
Didžiausias MRT rezultatų specifiškumas (iki 95–98 %) ir tikslumas pasiekiamas tiriant pacientus, kuriems yra vidutinė arba didelė ekstrakapsulinės invazijos rizika. Manoma, kad ekstrakapsulinė invazija (pagal MRT duomenis) rodo chirurginio gydymo netinkamumą ir nepalankią ligos prognozę. Hormoninė ar spindulinė terapija neturi įtakos prostatos naviko ekstrakapsulinio išplitimo nustatymo tikslumui. Pagrindinis sunkumas nustatant vėžio židinius ir ekstrakapsulinį naviko išplitimą yra didelis tomogramų interpretavimo kintamumas skirtingų specialistų. Pagrindinė spindulinės diagnostikos specialisto užduotis – pasiekti aukštą diagnostinį specifiškumą (net ir jautrumo sąskaita), kad operuojami pacientai neprarastų galimybės taikyti radikalų gydymą.
Dėl vėžinio, hiperplazinio ir normalaus prostatos audinio tankio panašumo atliekant KT tyrimą šis metodas mažai naudingas vertinant vietinį naviko išplitimą. Invazija į sėklines pūsleles yra svarbesnė nei invazija į kapsules, tačiau net ir šiuo atveju KT suteikia informacijos tik pažengusiais atvejais. Tačiau šis metodas aktyviai naudojamas smūgio sričiai pažymėti prieš spindulinę terapiją.
Lėtas spindulinės diagnostikos vystymasis mūsų šalyje lėmė vėlyvą prostatos vėžio diagnozavimą ir dėl to nepakankamą radikalių prostatos vėžio gydymo metodų (pvz., prostatektomijos) paplitimą, menką modernių tomografų prieinamumą ir tinkamų spindulinės diagnostikos specialistų bei urologų mokymo programų nebuvimą. Nepaisant to, kad KT ir MRT dabar yra plačiai paplitusios, kabinetų įrangos lygis ir spindulinės diagnostikos specialistų išsilavinimas yra nepakankamas, kad gauta informacija taptų lemiama renkantis prostatos vėžiu sergančių pacientų gydymo metodą.
Regioniniai limfmazgiai (N)
Regioniniai limfmazgiai turėtų būti vertinami tik tada, kai tai tiesiogiai veikia gydymo strategiją (dažniausiai planuojant radikalų gydymą). Didelis PSA kiekis, T2c -T3a navikai, prasta diferenciacija ir tarpvietės invazija yra susiję su didele limfmazgių metastazių rizika. Limfmazgių būklės įvertinimas pagal PSA kiekį laikomas nepakankamu.
Reikiamą informaciją suteikia tik limfadenektomija (atvira arba laparoskopinė). Naujausi išplėstinės limfadenektomijos tyrimai parodė, kad prostatos vėžys ne visada pažeidžia obturatorių limfmazgius. Esant besimptomiams navikams ir PSA lygiui mažesniam nei 20 kg/ml. KT patvirtina padidėjusius limfmazgius tik 1% atvejų. MRT arba KT naudojimas pateisinamas esant didelei metastazių rizikai, nes šių metodų specifiškumas siekia 93–96%. Tačiau net ir teigiamas rezultatas juos taikant gali būti klaidingas, ir tik įtartino limfmazgio punkcija leidžia atsisakyti limfadenektomijos. Remiantis retrospektyvia analize, limfmazgio dydis ne visada rodo metastazių buvimą jame; pažeistų limfmazgių asimetrija laikoma informatyvesniu požymiu. Šiuo metu tik 2–3% pacientų, kuriems atlikta radikali prostatektomija dėl lokalizuoto prostatos vėžio, pooperacinio histologinio tyrimo metu diagnozuojamos metastazės limfmazgiuose.
Rekomenduojami pozitronų emisijos tomografijos (PET) ir scintigrafijos su žymėtais antikūnais metodai metastazėms limfmazgiuose aptikti, tačiau jų taikymas vis dar ribotas dėl nepakankamo jautrumo.
Partino nomogramos (2001 m.) gali būti naudojamos regioninių limfmazgių pažeidimo rizikai įvertinti. Nomogramos yra matematiniai algoritmai, naudojami konkrečiam pacientui arba pacientų grupei. Šios lentelės leidžia nustatyti vietinio naviko išplitimo (į kapsulę, sėklines pūsleles) ir limfmazgių pažeidimo tikimybę, remiantis klinikine stadija, PSA lygiu ir Gleason indeksu. Visų pirma, jos leidžia nustatyti pacientų grupę, kuriai maža (mažiau nei 10 %) limfmazgių metastazių tikimybė (PSA lygis didesnis nei 20 ng/md, T1-2a stadija ir Gleason indeksas 2-6); šioje grupėje limfmazgių būklė prieš radikalų gydymą gali būti nenurodyta. Limfmazgių metastazių riziką taip pat galima įvertinti nustatant naviko sritis su ryškia anaplazija (4-5 balai): jei tokios sritys randamos keturiose ar daugiau biopsijų arba jos vyrauja bent vienoje biopsijoje, rizika siekia 20-45 %. Kitiems pacientams ji neviršija 2,5 %. Tokiais atvejais papildomo tyrimo nereikia.
Tolimos metastazės (M)
85 % pacientų, mirštančių nuo prostatos vėžio, nustatomi ašinio skeleto pažeidimai. Kaulų metastazės atsiranda dėl vėžio ląstelių patekimo į kaulų čiulpus su krauju, dėl ko atsiranda naviko augimas ir kaulų struktūrų lizė. Kaulų metastazių paplitimas turi įtakos prognozei, o ankstyvas jų nustatymas įspėja gydytoją apie galimas komplikacijas. 70 % atvejų metastazės yra derinamos su šarminės fosfatazės (ŠF) kaulų izofermento aktyvumo padidėjimu. ŠF aktyvumo ir PSA lygio nustatymas didžiąja dauguma atvejų leidžia aptikti kaulų metastazes. Remiantis daugiamatės analizės duomenimis, šiems rodikliams įtakos turi tik kaulų metastazių skaičius. Svarbu, kad kaulų izofermento ŠF aktyvumas tiksliau atspindėtų kaulų pažeidimo laipsnį nei PSA lygis.
Scintigrafija laikoma jautriausiu kaulų metastazių nustatymo metodu (ji pranašesnė už radiografiją ir šarminės bei rūgštinės fosfatazės aktyvumo nustatymą). Technecio difosfonatai geriau naudojami kaip radiofarmaciniai vaistai, nes jų kaupimasis kauluose yra daug aktyvesnis nei minkštuosiuose audiniuose. Nustatyta koreliacija tarp pusiau kiekybinio kaulų pažeidimo įvertinimo ir išgyvenamumo. Tolimų metastazių aptikimas galimas bet kuriame organe. Dažniausiai jos pasireiškia neregioniniuose limfmazgiuose, plaučiuose, kepenyse, smegenyse ir odoje. Esant atitinkamiems nusiskundimams ir simptomams, joms nustatyti naudojama krūtinės ląstos rentgenografija, ultragarsas, KT ir MRT. Įtariamų kaulų metastazių taktika pateikta diagramoje.
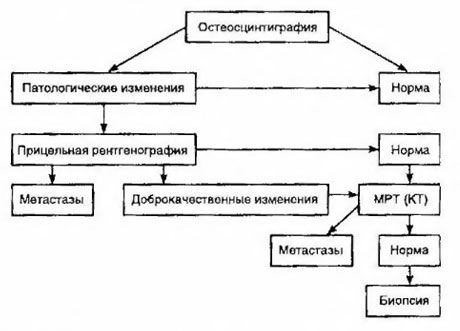
Patikimiausias laboratorinis rodiklis, padedantis nustatyti metastazių laipsnį, yra PSA lygis. Įrodyta, kad jo padidėjimas virš 100 ng/ml yra vienintelis parametras, patikimai rodantis tolimas metastazes. PSA lygio nustatymas sumažina pacientų, kuriems reikalinga kaulų scintigrafija, skaičių. Kaulų metastazių aptikimo tikimybė sumažėjus PSA lygiui yra labai maža. Nesant nusiskundimų ir pradiniam PSA kiekiui esant mažesniam nei 20 ng/ml, galima išvengti labai ir vidutiniškai diferencijuotų navikų nustatymo, scintigrafijos. Tuo pačiu metu, esant blogai diferencijuotiems navikams ir kapsulės invazijai, scintigrafija indikuotina (nepriklausomai nuo PSA lygio).


 [
[