Medicinos ekspertas
Naujos publikacijos
Vaistiniai preparatai
Vaistai, apsaugantys nuo trombozės ir gerinantys kraujo reologiją
Paskutinį kartą peržiūrėta: 07.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
Siekiant išvengti daugybinių mikrotrombų susidarymo šoko metu ir jų sunaikinimo, gali būti taikomi įvairūs farmakologiniai metodai, kuriuose naudojami vaistai, kurie neleidžia susidaryti trombams ir pagerina kraujo reologiją:
- sisteminių hemodinamikos ir mikrocirkuliacijos sutrikimų pašalinimas naudojant vazoaktyvius ir inotropinius agentus;
- priemonės kraujo reologijai gerinti naudojant racionalią infuzinę terapiją ir vaistus, kurie atkuria eritrocitų membranų elastingumą (trental arba pentoksifilinas);
- trombocitų agregacijos prevencija ir pradinių „baltųjų“ trombų susidarymas mažuose arteriniuose induose, vėliau inicijuojant krešėjimo kaskadą;
- trombų susidarymo slopinimas aktyvavus sisteminę krešėjimo kaskadą;
- fibrinolizės aktyvavimas siekiant ištirpinti naujai susidariusius kraujo krešulius (fibrinolizinas, streptokinazė, streptodekazė, urokinazė ir kt.) arba, priešingai, fibrinolizės slopinimas, kai ji generalizuota kai kuriems pacientams, sergantiems trauminiu šoku ir sepsiu (aminokaprono rūgštis, ambenas, kontrakalas ir kt.).
Dauguma išvardytų metodų yra tradiciniai, gerai išvystyti šoko gydymo praktikoje, turi savo hemorheologines indikacijas ir yra nurodyti atitinkamuose skyriuose. Todėl šiame skyriuje patartina išsamiau aptarti bendrą požiūrį į trombų susidarymo prevenciją šoko metu, naudojant farmakologinius preparatus, kurie veikia kraujo krešėjimo profazę. Būtent šis krešėjimo komplikacijų – „baltųjų arterijų trombų“ atsiradimo, susidarymo ir augimo – prevencijos lygis sulaukia didžiausio tyrėjų dėmesio.
Skirtingiems šoko tipams būdingi įvairūs ir dažnai daugiakrypčiai kraujo krešėjimo sutrikimai, pablogėjant jo reologinėms savybėms. Būdingiausias septinio, endotoksinio, nudegimo, trauminio ir hemoraginio tipo šoko požymis yra daugybinių mikrotrombų susidarymas mažiausiuose induose, kurį sukelia sisteminės hemodinamikos sutrikimai, kraujagyslių spazmai ir mikrocirkuliacijos sutrikimai, kraujo tirštėjimas, nuosėdos, sumažėjęs eritrocitų membranų elastingumas, taip pat daugybė bendrųjų ir vietinių veiksnių (autokoidų), inicijuojančių vietinius krešėjimo hemostazės pokyčius ir kraujo krešėjimo profazės įtraukimą.
Schema (sutrumpinta) forma pateikia pradinį hemokoaguliacijos etapą ir vietinės hemokoaguliacijos homeostazės mechanizmą taip.
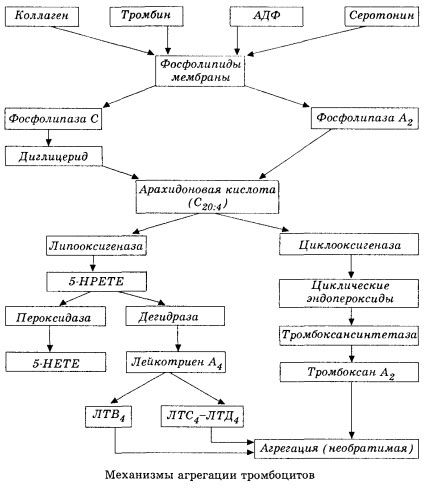
Jis prasideda nuo membraninės fosfolipazės A2 aktyvacijos dėl žalingų veiksnių derinio (tiesioginio membranos pažeidimo, hipoksijos, lipidų peroksidacijos, endogeninių cheminių veiksnių poveikio ir kt.). Dėl membraninių fosfolipidų skaidymosi išsiskiria neesterifikuotos ilgos grandinės riebalų rūgštys, iš kurių svarbiausia yra arachidono rūgštis kaip pradinis substratas. Jos transformacija (arachidono rūgšties kaskada) vyksta lipoksigenazės (leukotrienų sintezė) ir ciklooksigenazės (prostaglandinų, tromboksanų, prostaciklino sintezė) keliais.
Susidarę leukotrienai (B4, C4, E4, D4 ir kt.) – itin didelio biologinio aktyvumo medžiagos, tarp kurių yra ir lėtai reaguojanti anafilaksijos medžiaga – yra labai svarbios inicijuojant vietines kraujagyslių, uždegimines ir imunines reakcijas, įskaitant autoimuninius procesus. Leukotrienai sukelia mikrocirkuliacijos sutrikimus, padidina kraujo krešėjimą, išsiskiria autoliziniai lizosominiai fermentai ir į kraują išsiskiria faktorius, slopinantis miokardo susitraukimą ir bronchų spazmą.
Dėl savo gebėjimo sukelti lygiųjų raumenų susitraukimą, leukotrienai reikšmingai veikia sisteminę hemodinamiką, vainikines kraujagysles ir miokardą, sukeldami galingą vainikinių arterijų susitraukimą ir neigiamą inotropinį poveikį, kurį lydi širdies išstūmimo sumažėjimas ir kuris vaidina svarbų vaidmenį hipotenzijos vystymesi.
Sumažėjęs širdies išstūmis ir hipotenzinis atsakas į leukotrienus yra susiję su širdies raumens susilpnėjimu ir veninio kraujo grįžimo į širdį apribojimu. Didelę reikšmę veninio kraujo grįžimo ribojimui turi leukotrienų gebėjimas padidinti kraujagyslių sienelių pralaidumą ir sukelti plazmos ekstravazaciją. Leukotrienai laikomi svarbiais miokardo infarkto patogenezėje.
Anafilaksinio ir septinio (endotoksino) šoko atveju jų vaidmuo, matyt, dar labiau padidėja, ką rodo leukotrienų gebėjimas dideliais kiekiais kauptis plazmoje alerginių reakcijų metu ir sukelti anafilaksiniam šokui būdingus sisteminės kraujotakos pokyčius, taip pat leukotrienų receptorių blokatorių ir lipoksigenazės inhibitorių apsauginis poveikis. Selektyvių leukotrienų receptorių blokatorių kūrimas vyksta gana intensyviai ir yra perspektyvi mokslo kryptis. Šioje srityje jau pasiekta tam tikros sėkmės, o tokių blokatorių veiksmingumas miokardo išemijos, endotoksino ir hemoraginio šoko atveju yra eksperimentiškai patvirtintas. Tačiau tikriausiai prireiks dar kelerių metų, kol ši kryptis bus kliniškai įgyvendinta.
Jei veninėse kraujagyslėse trombai susidaro vienodai dalyvaujant trombocitams ir plazmos krešėjimo faktoriams, tai arterijose trombocitai yra pagrindiniai proceso iniciatoriai. Juose yra ADP, Ca2+, serotonino, fosfolipidų, prostaglandinų ir tromboksano sintezės fermentų, trombostenino (kaip ir raumenų aktomiozinas suteikia šioms ląstelėms susitraukimo gebėjimą), epitelio ir raumenų kraujagyslių sienelių ląstelių trombogeninio augimo faktoriaus ir daugelio kitų medžiagų. Humoralinis trombocitų funkcijų reguliavimas atliekamas per specializuotus jų membranų receptorius (alfa2 ir beta2 adrenoreceptorius, histamino ir serotonino receptorius, acetilcholiną, tromboksaną, adenoziną ir daugelį kitų). Ypatinga trombocitų savybė yra didelis afinitetas kolagenui ir kitiems subendoteliniams kraujagyslių sienelių elementams, nešlapiems ir neigiamai įkrautiems paviršiams. Ši savybė suteikia trombocitams išskirtinį gebėjimą prilipti (prilipti) prie pažeisto endotelio indo dalies, kuri šoko metu turi didelę tikimybę būti pažeista. Šiuo atveju trombocitai išsisklaido ir išskiria pseudopodijas, kurios gali prilipti viena prie kitos ir prie kraujagyslės sienelės. Padidėja membranos pralaidumas, iš trombocitų išsiskiria ADP, serotoninas, tromboksanas ir kai kurie trombocitų paviršiuje adsorbuoti krešėjimo faktoriai. Šios medžiagos sąveikauja su atitinkamais membranos receptoriais ir, dalyvaujant kalcio jonams, sukelia agregaciją (iš pradžių grįžtamąją). Procesas tampa savarankiškas, kurį palengvina humoraliniai reguliavimo veiksniai; kiti veiksniai, priešingai, gali jį sustabdyti ir netgi panaikinti, sukeldami dezagregaciją.
Vyraujant trombus formuojantiems veiksniams ir sąlygoms, sukibimo ir grįžtamosios agregacijos fazes pakeičia trečioji fazė – negrįžtama agregacija, kuri vykdoma dalyvaujant trombosteninui ir sukelia krešulio susiaurėjimą; agreganto sustiprėjimo ir susitraukimo reakcija taip pat vyksta dalyvaujant Ca+, ATP ir sukelia balto trombo susidarymą.
Ciklooksigenazės būdu vykstanti arachidono rūgšties konversija trombocituose, kraujagyslių endotelio ląstelėse ir kituose audiniuose užtikrina vietinę (metabolitų pusinės eliminacijos laikas yra labai trumpas) krešėjimo homeostazę, nes šio metabolizmo metu susidaro galingos pro- ir antiagregantinės medžiagos. Pagrindinis trombocitų agregaciją aktyvuojantis veiksnys ciklooksigenazės reakcijų grandinėje yra tromboksanas A2, o ne mažiau galingas jo antagonistas yra prostaciklinas, kurį gamina endotelio ląstelės, ir, mažesniu mastu, E ir G serijos prostaglandinai. Galiausiai, trombocitų agregaciją stipriai veikia papildomi vietiniai ir sisteminiai humoraliniai veiksniai.
Trombocitų agregacijos aktyvatoriai ir inhibitoriai
Trombocitų agregacijos iniciatoriai ir aktyvatoriai |
Trombocitų agregacijos inhibitoriai |
Kolagenas |
- |
ADP |
Adenozinas ir jo stabilizatoriai |
Norepinefrinas (per alfa2 receptorius) |
Alfa adrenerginius blokatorius |
Serotoninas |
Antiserotonino agentai |
Histaminas |
Antihistamininiai vaistai |
Trombinas |
Heparinas |
Ca2+ |
Ca2+ antagonistai |
CGMP – jo induktoriai (acetilcholinas?) ir stabilizatoriai |
CAM – jo induktoriai (per beta adrenerginius receptorius) ir stabilizatoriai (fosfodiesterazės inhibitoriai) |
Arachidono rūgštis |
Dekstransai, albuminas |
Tromboksanas A2 |
Prostaciklinas I2 |
Farmakologinės intervencijos pradinėje trombų susidarymo fazėje šoko ir ūminių išeminių procesų metu širdyje ir smegenyse rodo tokią galimybę:
- arachidono rūgšties kaskados pradinių reakcijų (visiškos ir dalinės) slopinimas;
- tam tikros tromboksano sintezės reakcijos slopinimas;
- leukotrienų ir tromboksanų receptorių blokada trombocituose, lygiuosiuose raumenyse ir kitose ląstelėse;
- medžiagų, kurios moduliuoja trombocitų agregaciją, t. y. kitaip silpnina pastarųjų reakciją į inicijuojančių veiksnių (kolageno, tromboksano A2, leukotrienų ir kt.) įtaką, vartojimas.
Įgyvendinant išvardintus kraujo reologinių savybių sutrikimų korekcijos metodus, išsprendžiama pagrindinė taktinė užduotis: apsaugoti trombocitų agregacijos ir adhezijos receptorius nuo aktyvatorių poveikio arba slopinti šių receptorių sintezės tarpląstelinius mechanizmus. Pradinių arachidono rūgšties kaskados reakcijų slopinimas gali būti pasiektas apsaugant trombocitų receptorius, reaguojančius į polimerinius aktyvatorius, naudojant mažos molekulinės masės dekstranus, kurių molekulės konkuruoja su fibrinu, kolagenu, agreguotu imunoglobulinu (IgE) ir komplemento sistemos komponentais.
Maskuodami trombocitų membranos receptorius ir konkuruodami su stambiai išsisklaidžiusiais baltymais eritrocitų paviršiuje, mažos molekulinės masės dekstranai juos išstumia ir sunaikina tiltelius tarp ląstelių. Taip yra dėl to, kad dekstranai, apgaubdami kraujagyslių endotelį ir kraujo ląstelių elementų paviršių, padidina jų neigiamą krūvį, taip sustiprindami antiagregacines savybes.
Dekstransas
Mažos molekulinės masės dekstranai mažina kolageno ir ADP sukeltą trombocitų agregaciją, taip pat trombino aktyvinantį poveikį trombocitams, slopina pradinio baltojo trombocitų trombo augimą, gerina kraujotaką, mažina pooperacinį plazmos fibrinogeno kiekio padidėjimą, keičia fibrino struktūrą ir stabilumą.
Į veną leidžiami dekstranai traumos ir šoko atveju ne tik sumažina trombocitų agregaciją ir sukibimą, bet ir mobilizuoja endogeninį hepariną, taip skatindami laisvo ir sunkiai įtraukiamo kraujo krešulio susidarymą, kurį lengvai lizuoja fibrinolitikai. Mažos molekulinės masės dekstranų antitrombino aktyvumas yra susijęs su jų specifiniu poveikiu kraujo krešėjimo VIII faktoriaus struktūrai ir funkcijai. VIII faktorius (antihemofilinis globulinas) – didelė molekulė, turinti sudėtingą struktūrą ir funkciją, – dalyvauja trombocitų agregacijoje ir susidariusio krešulio stabilume. Dekstranai trukdo VIII faktoriaus veikimui, taip sulėtindami trombocitų agregaciją ir sumažindami krešulio stabilumą.
Mažos molekulinės masės dekstranai nėra tikri antikoaguliantai, o jų korekcinis poveikis hemoreologiniams sutrikimams daugiausia susijęs su hemodilucija, cirkuliuojančios plazmos tūrio papildymu ir kraujotakos pagerėjimu mikrocirkuliacijos sistemoje.
Dekstranų gebėjimas pagerinti kraujotaką esant hemodinaminiams sutrikimams (šokui, kraujo netekimui) priklauso nuo daugelio veiksnių. Didelė trumpalaikė polimero koncentracija kraujyje ne tik sukelia „tiesioginę hemodiluciją“, bet ir sudaro sąlygas skysčiui tekėti į kraują iš intersticinės erdvės ir vėlesniam dekstrano osmosinio poveikio subalansavimui. Dėl hemodilucijos sumažėja kraujo klampumas, padidėja veninis kraujo pritekėjimas į širdį ir širdies išstūmimas. Kartu su šiuo poveikiu dekstranai sudaro kompleksus su fibrinogenu ir turi antilipeminį poveikį.
Taigi, mažos molekulinės masės dekstranų antiagregacinis ir hemodinaminis poveikis padeda sumažinti kraujo klampumą, o tai ypač svarbu esant mažam šlyties greičiui. Kraujo ląstelių dezagregacija pagerina sisteminę kraujotaką ir mikrocirkuliaciją, ypač veninėje jos dalyje, kur greičio gradientai yra mažiausi. Mažos molekulinės masės dekstranų tirpalų naudojimas esant įvairiems šoko tipams, chirurginio traumų ir jų pasekmių gydymo metu, o vėliau pooperaciniu laikotarpiu padeda išvengti hiperkoaguliacijos ir sumažinti trombozinių procesų bei embolijų tikimybę.
Tačiau reikia pažymėti, kad kai kuriais atvejais dekstrano tirpalų infuzijos lydi anafilaksines ir alergines reakcijas (pavojingos esant sensibilizacijai ir anafilaksiniam šokui). Taip yra dėl to, kad dekstranai, turintys didelę molekulinę masę ir daug šoninių grandinių, gali veikti kaip antigenas. Todėl, norint nustatyti individualų jautrumą, rekomenduojama iš anksto į veną suleisti iki 20 ml mažos molekulinės masės dekstrano tirpalo kaip hapteno (15% tirpalas, molekulinė masė 1000) ir prieš anestezijos įvedimą atlikti plazmos pakaitalo infuzijas.
 [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ]
[ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ]
Trombino inhibitoriai
Farmakologinė trombocitų receptorių, sąveikaujančių su trombocitų aktyvatoriais, apsauga taip pat gali būti pasiekta naudojant agentus, kurie konkuruoja su nepolimeriniais trombocitų aktyvatoriais arba juos slopina. Tokie agentai yra trombino inhibitoriai (heparinas ir hirudinas, nemažai sintetinių inhibitorių, adrenalino antagonistai), alfa receptorių blokatoriai (fentolaminas, dihidroergotaminas), ADP antagonistai (dipiridamolis, adenozinas ir jo struktūriniai analogai, fosfokreatinas), serotonino antagonistai (metisergidas). Tik keli iš išvardytų agentų yra naudojami įvairios kilmės šoko profilaktikai ir gydymui.
Įvairių grupių vaistais galima apsaugoti baltymų receptorių, reaguojančių su trombocitų agregacijos ir adhezijos aktyvatoriais, sintezės tarpląstelinius mechanizmus ir slopinti tromboksano sintezės procesus:
- cATP, prostaciklino ir prostaglandino PgE2 induktoriai ir stabilizatoriai;
- fosfolipazės ir fosfodiesterazės inhibitoriai.
Intensyvus specialių antitrombocitinių vaistų kūrimas prasidėjo palyginti neseniai ir kol kas nedavė patikimų rezultatų. Šiuo metu klinikinėje praktikoje, be dekstrano tirpalų, baltųjų trombocitų trombams susidaryti išvengti plačiai naudojami tokie antitrombocitiniai vaistai kaip acetilsalicilo rūgštis, indometacinas, dipiradamolis, sulfinpirazonas (persantinas), prostaciklinas (eikoprostenonas) ir heparinas.
Nesteroidiniai vaistai nuo uždegimo
Nustatyta, kad nesteroidinių vaistų nuo uždegimo – acetilsalicilo rūgšties ir indometacino – farmakologinis poveikis atsiranda dėl jų poveikio eikozanoidų (tromboksanų ir prostaglandinų) metabolizmui. Beveik visi šios grupės vaistai slopina fermentų kompleksą, žinomą kaip prostaglandinų sintetazė, tokiu būdu sukeldami savo specifinį ir antiagregantinį poveikį.
Išgerta acetilsalicilo rūgštis absorbuojama labai greitai. Jos hidrolizės produktas, salicilo rūgštis, slopina trombocitų ciklooksigenazę, o tai sutrikdo arachidono rūgšties virtimą prostaglandinu O2 ir galiausiai tromboksanu A2. Acetilsalicilo rūgštis slopina kolageno, ADP, adrenalino ir serotonino sukeltą agregaciją. Nors jos GG0 5 yra 15 minučių, antiagregantinis poveikis trunka kelias dienas, kas, matyt, paaiškinama negrįžtamu prostaglandinų sintezės reakcijų slopinimu ir trombocitų agregacijos funkcijos slopinimu per visą jų gyvenimą (6–10 dienų). Kartu su trombocitų ciklooksigenazės slopinimu, didelėmis dozėmis acetilsalicilo rūgštis slopina kraujagyslių sienelių ciklooksigenazę ir kartu slopindama tromboksano A2 sintezę slopina prostaciklinų sintezę endotelio ląstelėse. Todėl acetilsalicilo rūgštis kaip antiagregantas turėtų būti skiriama mažomis dozėmis (3000–5000 mg/d.), kurios daugiausia slopina trombocitų agregaciją.
Atsižvelgiant į tai, kad acetilsalicilo rūgštis kelias dienas blokuoja trombocitų ciklooksigenazę, o endotelio ciklooksigenazę – ne ilgiau kaip parą, vaistą racionalu skirti ne kasdien, o kas 3–4 dienas. Optimali acetilsalicilo rūgšties dozė pacientui turėtų būti parenkama individualiai, nes pacientų jautrumas antitrombocitiniam vaisto poveikiui yra skirtingas. Reaktyviems pacientams 0,5 g acetilsalicilo rūgšties dozė slopina trombocitų agregaciją 40–50 %, hiperreaktyviems – visiškai arba 80–90 %, o reaktyviems pacientams vartojant tą pačią vaisto dozę, antitrombocitinio poveikio nėra.
Selektyvūs tromboksano sintetazės inhibitoriai yra imidazolas ir jo analogai, kurie neblokuoja ciklooksigenazės. Dipiridamolis, klinikinėje praktikoje naudojamas lėtinei išeminei širdies ligai gydyti kaip vainikinių arterijų plečiantis vaistas, kaip ir imidazolas selektyviai slopina tromboksano sintetazę, neleisdamas sintezuoti tromboksano A2. Manoma, kad vaistas ir jo analogai taip pat slopina trombocitų fosfodiesterazę, taip padidindami cAMP koncentraciją trombocituose. Kartu su tuo dipiridamolis slopina adenozino deaminazės aktyvumą ir adenozino pasisavinimą trombocituose, blokuoja serotonino absorbciją trombocituose ir jų agregaciją, kurią sukelia adrenalinas ir kolagenas. Yra pranešimų apie silpną vaisto antitrombocitinį aktyvumą ir jo gebėjimą mažomis dozėmis sustiprinti trombocitų agregaciją. Patikimiausias antitrombocitinis poveikis gali būti pasiektas vartojant dipiridamolio ir acetilsalicilo rūgšties derinį.
Heparinas
Tarp antitrombozinių vaistų vienas veiksmingiausių kraujo agregato būsenos reguliatorių yra heparinas, ypač vartojamas anksti. Heparinas turi didelį neigiamą krūvį ir gali sąveikauti tiek su dideliais, tiek su mažais jonais ir molekulėmis (fermentais, hormonais, biogeniniais aminais, plazmos baltymais ir kt.), todėl jo biologinio poveikio spektras yra gana platus. Vaistas pasižymi antitrombino, antitromboplastino ir antiprotrombino poveikiu, neleidžia fibrinogenui virsti fibrinu, slopina krešulio retrakciją ir didina fibrinolizę.
Heparino antikoaguliacinio veikimo mechanizmas yra gana sudėtingas. Dabar nustatyta, kad heparino antikoaguliacinis poveikis yra susijęs su antitrombino III veikimo sustiprinimu ir heparino-antitrombino III komplekso gebėjimo greitai inaktyvuoti daugumą kraujo krešėjimo sistemos serino proteazių padidėjimu. Heparino antitromboziniam poveikiui didelę reikšmę turi jo gebėjimas padidinti ir palaikyti aukštą kraujagyslių intimos elektroneigiamą potencialą, užkertant kelią trombocitų adhezijai ir trombocitų mikrotrombų susidarymui. Heparinas aktyviausiai slopina trombų susidarymą venose, užkirsdamas kelią tiek vietiniam trombų susidarymui, tiek diseminuotai intravaskulinei koaguliacijai.
Prostaciklinas ir jo stabilūs analogai
Tarp antitrombocitinių vaistų stipriausi agregacijos inhibitoriai yra prostaciklinas ir jo stabilūs analogai. Prostaciklino antitrombocitinis poveikis atsiranda dėl adenilato ciklazės stimuliavimo ir dėl to cAMP koncentracijos padidėjimo trombocituose, tromboksano kiekio sumažėjimo, tromboksano A2 kiekio sumažėjimo ir jo receptorių blokados. Prostaciklinas yra nestabilus ir greitai hidrolizuojamas į neaktyvius produktus, todėl jis lašinamas į veną 2–20 ng/kg per minutę greičiu 30–60 minučių iki 6 kartų per dieną.
Prostaciklinas, kartu su stipriu antiagregaciniu poveikiu, pasižymi stipriu kraujagysles plečiančiu ir bronchus plečiančiu poveikiu. Vaistas plečia smegenų, širdies, inkstų, griaučių raumenų ir mezenterinių kraujagyslių kraujagysles. Veikiant prostaciklinui, padidėja vainikinių arterijų kraujotaka, padidėja miokardo energijos tiekimas ir sumažėja jo deguonies poreikis. Nepaisant nestabilumo organizme, kliniškai palankus poveikis gali trukti kelias savaites ir net mėnesius. Tokio užsitęsusio veikimo mechanizmas dar nėra aiškus.
Prostaciklinas yra mažai toksiškas vaistas, tačiau jo vartojimas gali sukelti šalutinį poveikį: veido paraudimą, galvos skausmą, sumažėjusį kraujospūdį, pilvo skausmą, anoreksiją. Kartu su prostaciklinu, perspektyvūs trombocitų agregacijos inhibitoriai yra jo sintetiniai stabilūs analogai (iloprostas ir kt.).
Vaistai, kurie pagerina kraujo klampumą
Kraujo reologinių savybių sutrikimus traumos ir šoko metu sukelia ne tik trombocitų funkcinio aktyvumo pokyčiai, bet ir padidėjęs kraujo klampumas. Kraujo, kaip sudėtingos dinaminės dispersinės sistemos, struktūrinį klampumą daugiausia lemia plazmos klampumas ir eritrocitų gebėjimas deformuotis. Plazmos klampumas daugiausia priklauso nuo baltymų koncentracijos kraujyje. Mažos molekulinės masės baltymai, pavyzdžiui, albuminas, mažai veikia plazmos klampumą, o didelės molekulės baltymai (fibrinogenas, alfa ir gama globulinai, kitos makromolekulės) jį žymiai padidina.
Esant mažam šlyties greičiui, fibrinogeno ir globulinų adsorbcija ant eritrocitų paviršiaus lemia tiltelių susidarymą tarp gretimų ląstelių ir agregatų susidarymą iš eritrocitų. Agregatų susidarymo greitis yra sudėtingas biofizinis procesas ir priklauso ne tik nuo šlyties dydžio, bet ir nuo eritrocitų elektrokinetinių savybių, makromolekulių-agregatorių koncentracijos, masės ir sorbcijos pajėgumo, nuo eritrocitų formos ir plastiškumo.
Eritrocitų membranos formos ir mechaninių savybių palaikymui reikia didelių energijos sąnaudų. Manoma, kad glikolizės metu eritrocituose gaminama energija sunaudojama spektrino fosforilinimui, dėl ko pakinta baltymo antrinė struktūra ir jis sąveikauja su gretimais vidinės membranos komponentais. Membranos struktūrinių baltymų, spektrino ir aktino, sąveika vaidina svarbų vaidmenį formuojant eritrocitų membranos mechanines savybes, palaikant pastovų eritrocitų paviršiaus plotą ir jo storį bet kokios deformacijos metu.
Esant sisteminiams hemodinamikos ir organų kraujotakos sutrikimams, padidėjęs eritrocitų membranų standumas ir eritrocitų agregatų susidarymas sumažina eritrocitų praėjimo per kapiliarus greitį, taip sutrikdydamas kraujo dujų pernašos funkciją. Todėl šoko metu susidariusių kraujo reologinių savybių sutrikimų korekcija turėtų apimti ne tik eritrocitų agregacijos prevenciją, bet ir plazmos bei kraujo klampumo, eritrocitų agregacijos ir deformacijos normalizavimą.
Be mažos molekulinės masės dekstranų, albumino tirpalai yra viena iš veiksmingų priemonių kraujo suspensijos stabilumui didinti. Vėlyvuoju šoko laikotarpiu, sumažėjus albumino koncentracijai kraujo plazmoje ir padidėjus fibrinogeno bei globulinų, ypač alfa2 frakcijos, lipoproteinų ir lipidų, koncentracijai, atsiranda generalizuota eritrocitų agregacija. Tokiomis sąlygomis reologinis albumino poveikis atsiranda dėl dviejų pagrindinių veiksnių: hemodilucijos ir mikro- ir makroglobulinių baltymų santykio plazmoje normalizavimo. Tuo pačiu metu albuminas jungiasi su laisvosiomis rūgštimis, kurių labilizacija traumos ir šoko metu stimuliuoja kraujo ląstelių struktūrų agregaciją ir intravaskulinę koaguliaciją bei gali sukelti riebalų emboliją.
Antišoko priemonės, kuriomis siekiama papildyti cirkuliuojančio kraujo tūrį, pašalinti audinių hipoksiją ir metabolinę acidozę, prisideda prie eritrocitų membranų elastingumo normalizavimo, nes hipoksija ir acidozė žymiai sumažina eritrocitų deformuojamumą. Padidėjęs eritrocitų membranų standumas šoko metu greičiausiai susijęs su ATP sintezės slopinimu eritrocituose. Savo ruožtu, ATP koncentracijos sumažėjimas prisideda prie Ca2+ koncentracijos padidėjimo eritrocituose, kuris, prisijungdamas prie membranos baltymų, padidina membranos standumą.
Vienas iš farmakologinių vaistų, didinančių ATP kiekį eritrocituose ir eritrocitų membranų elastingumą, yra Trental (pentoksifilinas), kuris klinikinėje praktikoje naudojamas išeminiams sutrikimams gydyti.
Kartu su eritrocitų membranų standumo mažinimu Trental sukelia vazodilataciją, pagerina audinių aprūpinimą deguonimi, slopina fosfodiesterazės aktyvumą audiniuose, padidina cAMP koncentraciją ir slopina trombocitų agregaciją.
Tarp kitų farmakologinių preparatų, palaikančių eritrocitų membranos elastingumą, verta paminėti Ca2+ antagonistus, kurie riboja jonų patekimą į eritrocitus (flunarizinas, nifedipinas ir kt.).
 [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
[ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
Dėmesio!
Siekiant supaprastinti informacijos suvokimą, ši vaisto "Vaistai, apsaugantys nuo trombozės ir gerinantys kraujo reologiją" naudojimo instrukcija yra išversta ir pateikta specialioje formoje remiantis oficialiais vaisto vartojimo medicinos tikslais instrukcijomis. Prieš naudodami perskaitykite anotaciją, kuri buvo tiesiogiai prie vaisto.
Aprašymas pateikiamas informaciniais tikslais ir nėra savirealizacijos vadovas. Šio vaisto poreikis, gydymo režimo tikslas, metodai ir vaisto dozė nustatoma tik gydantis gydytojas. Savarankiškas gydymas yra pavojingas jūsų sveikatai.

