Medicinos ekspertas
Naujos publikacijos
Poūmis de Kvereno tiroiditas.
Paskutinį kartą peržiūrėta: 12.07.2025

Visas „iLive“ turinys yra peržiūrėtas medicinoje arba tikrinamas, kad būtų užtikrintas kuo didesnis faktinis tikslumas.
Mes turime griežtas įsigijimo gaires ir susiejamos tik su geros reputacijos žiniasklaidos svetainėmis, akademinių tyrimų institucijomis ir, jei įmanoma, medicininiu požiūriu peržiūrimais tyrimais. Atkreipkite dėmesį, kad skliausteliuose ([1], [2] ir tt) esantys numeriai yra paspaudžiami nuorodos į šias studijas.
Jei manote, kad bet koks mūsų turinys yra netikslus, pasenęs arba kitaip abejotinas, pasirinkite jį ir paspauskite Ctrl + Enter.
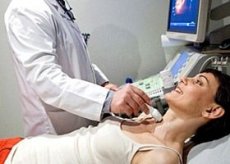
Subūminis de Quervain tiroiditas arba granulomatozinis tiroiditas yra viena iš labiausiai paplitusių ligos formų.
Rudens-žiemos laikotarpiu pastebimas ligų paplitimo padidėjimas. Moterys serga 4 kartus dažniau nei vyrai, pacientų amžius gali skirtis, tačiau didžiausias atvejų skaičius pasitaiko 30–40 metų amžiaus.
Priežastys poūmis de Kvereno tiroiditas.
Po tymų, infekcinio parotito, adenovirusinių ligų padaugėja poūmio tiroidito atvejų. Jis išsivysto praėjus 3–6 savaitėms po virusinių infekcijų. Įsiskverbęs į ląstelę, virusas sukelia netipinių baltymų susidarymą, į kuriuos organizmas reaguoja uždegimine reakcija.
 [ 5 ]
[ 5 ]
Pathogenesis
De Quervain tiroiditui būdingas simetriškas arba asimetriškas liaukos padidėjimas. Jos audinys tankus, pjūvyje matinis ir nevienalytės struktūros. Mikroskopiškai aptinkama daugybė granulomų, susidariusių iš milžiniškų ir pseudomilžiniškų ląstelių (histiocitų sankaupų aplink koloidinius lašus), iš folikulų išsiliejusio koloido, makrofagų, neutrofilų ir eozinofilų. Granulomų susidarymo vietose folikulai suyra, epitelis pleiskanoja ir yra nekrozinis.
Intersticiniame audinyje aplink ir tarp granulomų yra mukoidinė edema ir limfoidinė infiltracija, įskaitant plazmines ląsteles; randama makrofagų, eozinofilų ir putliųjų ląstelių. Nepažeistuose folikuluose ląstelės rodo padidėjusio funkcinio aktyvumo požymius, o pamatinė membrana sustorėja. Kartais granulomos pūliuoja, susidaro mikroabscesai. Laikui bėgant stebima ryški stromos fibrozė su kalkių nusėdimu, taip pat regeneraciniai procesai: naujų folikulų formavimasis tarpląstelinio epitelio salelėse ir sunaikintų folikulų ląstelėse.
Simptomai poūmis de Kvereno tiroiditas.
Jaučiamas ūmus negalavimas, skausmas kaklo srityje, plintantis į ausį, stiprėjantis ryjant ir judant. Kūno temperatūra pakyla iki 38–39 °C, bet gali būti ir subfebrilinė. Liauka padidėja (su difuziniu pažeidimu), atsiranda spaudimo jausmas priekiniame kaklo paviršiuje, sustiprėja silpnumas, prakaitavimas, nervingumas ir bendras negalavimas. Nuo pirmųjų ligos dienų klinikiniame kraujo tyrime pastebimas sparčiai didėjantis ESR – iki 60–80 mm/val. (kai kuriais atvejais iki 100 mm/val.) – su normaliu arba šiek tiek padidėjusiu leukocitų kiekiu, be kraujo formulės pokyčių.
Ligos eigą galima suskirstyti į kelis etapus, kurių metu gaunami skirtingi laboratorinių tyrimų rezultatai. Taigi, pirmojoje, ūminėje stadijoje (trunkančioje 1–1,5 mėn.), kraujyje padidėja alfa2-globulinų, fibrinogeno ir skydliaukės hormonų kiekis, sumažėja jodo izotopo pasisavinimas liaukoje. Kliniškai stebimi tireotoksikozės simptomai. Toks skenavimo duomenų ir klinikinių simptomų neatitikimas paaiškinamas tuo, kad uždegimo pažeista liauka praranda gebėjimą fiksuoti jodą; anksčiau susintetinti hormonai ir tireoglobulinas patenka į kraują dėl padidėjusio kraujagyslių pralaidumo uždegimo fone. Po 4–5 savaičių sutrikus hormonų sintezei, jų kiekis kraujyje normalizuojasi, o vėliau sumažėja.
Skausmas liaukoje mažėja ir išlieka tik palpuojant. ESR vis dar padidėja, alfa2-globulinų ir fibrinogeno kiekis išlieka padidėjęs. Sumažėjęs tiroksino ir trijodtironino kiekis suaktyvina skydliaukę stimuliuojančio hormono išsiskyrimą iš hipofizės ir padidina jodo izotopo pasisavinimą skydliaukėje. Maždaug iki 4 mėnesio nuo ligos pradžios pabaigos gali padidėti 1311 absorbcija, pasireiškiant vidutinio sunkumo klinikiniams simptomams, sausai odai. Šie reiškiniai praeina savaime, nes atsistato liaukos funkcija ir prasideda sveikimo stadija. Liaukos dydis normalizuojasi, skausmas išnyksta, ESR sumažėja, T4, T3 ir TSH rodikliai normalizuojasi. Spontaniškai tai trunka 6–8 mėnesius, tačiau liga linkusi atsinaujinti, ypač veikiant nepalankiems veiksniams (hipotermijai, nuovargiui, pasikartojančioms virusinėms infekcijoms).
Diagnostika poūmis de Kvereno tiroiditas.
Poūmio de Quervain tiroidito diagnozė nustatoma remiantis anamnezės duomenimis, klinikiniais simptomais, padidėjusiu ESR esant normaliam kraujo tyrimui, maža 1311 absorbcija skydliaukėje ir tuo pačiu metu dideliu skydliaukės hormonų kiekiu kraujyje, milžiniškų daugiabranduolių ląstelių buvimu punkcijos biopsijoje ir geru gliukokortikoidų gydymo poveikiu. Naudojant skydliaukės ultragarsą, kai stebimi specifiniai struktūriniai pokyčiai (echoneigiamos zonos be aiškių ribų, išnykstančios po 4–6 savaičių taikant priešuždegiminį gydymą), punkcijos biopsija naudojama retai. Skenavimas naudojamas tik įtarus piktybinį naviką.
 [ 8 ]
[ 8 ]
Ką reikia išnagrinėti?
Kaip patikrinti?
Diferencialinė diagnostika
Priklausomai nuo poūmio tiroidito stadijos, atliekama diferencinė diagnostika su įvairiomis ligomis. Pirmiausia reikia atskirti nuo ūminio pūlingo tiroidito, atidžiai išsiaiškinti iš paciento duomenis apie ankstesnes ligas, turint omenyje, kad virusinis tiroiditas pasireiškia daug dažniau nei pūlingas. Poūmiam tiroiditui būdingas labai padidėjęs ESR su normaliu leukocitų kiekiu be kraujo formulės pokyčių, padidėjęs alfa2-globulinų ir fibrinogeno kiekis. Papildomas argumentas šios ligos naudai yra tai, kad gydymas antibiotikais neduoda jokio poveikio 5-7 dienas.
Jei liga prasideda lėtai, be ryškaus kūno temperatūros pakilimo ir skausmo liaukoje, pacientas gali kreiptis į gydytoją tik hipertiroidizmo stadijoje, todėl būtina atskirti tiroiditą nuo pradinės difuzinio toksinio gūžio formos. Sergant difuziniu toksiniu gūžiu, klinikinis tireotoksikozės vaizdas sutampa su padidėjusia izotopo absorbcija liaukoje, dideliu skydliaukės hormonų kiekiu kraujyje ir mažu skydliaukę stimuliuojančio hormono kiekiu. Sergant tiroiditu, didelį hormonų kiekį kraujyje lydi mažas izotopo pasisavinimas ir normalus arba sumažėjęs TSH kiekis.
Esant klinikiniams hipotirozės simptomams, būtina atmesti autoimuninį tiroiditą. Tai padeda nustatyti klasikinius antitiroidinius kūnelius, kurių nustatymas dideliais titrais būdingas šiai ligai. Poūmio tiroidito atveju antikūnų prieš tireoglobuliną titrai kartais nustatomi neviršijant kelių šimtų. Mažas skydliaukės hormonų kiekis kraujyje sutampa su dideliu TSH kiekiu ir maža izotopo absorbcija liaukoje autoimuninio tiroidito atveju. Poūmio tiroidito atveju padidėjęs TSH kiekis yra susijęs su padidėjusia I absorbcija (atsigavimo stadijoje). Taip pat nurodoma punkcijos biopsija: būdingi morfologiniai pokyčiai leidžia tiksliau diagnozuoti.
Židininio ir židininio poūmio tiroidito atveju pažeidžiama liaukos skilties dalis, kuri palpuojant nustatoma kaip skausmingas sutankinimas. Šią tiroidito formą reikia diferencijuoti nuo karcinomos. Abiejų ligų atveju klinikiniai simptomai (skausmas, apšvitinimo taškai, dydis, tankis) neleidžia net preliminarios diagnozės nustatyti (anamneziniai duomenys apie buvusią virusinę infekciją gali būti vertingas papildymas). Iš papildomų tyrimo metodų būtina paminėti netiesioginę skydliaukės limfografiją, kai pacientui vertikalioje padėtyje į apatinius skilčių polius suleidžiama kontrastinė medžiaga.
Po 60 minučių liauka kontrastuojama. Tiroidito rentgenografijai būdingas liaukos struktūros pokytis, kuris įgauna stambių granulių ir plyšusių trabekulų formą. Sergant tiroiditu, regioniniai limfmazgiai kontrastuojami po 24 valandų, o sergant karcinoma – užsikimšę. Pasak S. J. Serpuchovitino, skydliaukės limfografijos duomenys 93 % atvejų sutampa su histologinio tyrimo rezultatais. Taip pat indikuotina punkcijos biopsija, dėl kurios nėra sutarimo.
Vis dėlto dauguma autorių pritaria šiam diagnostiniam metodui. Specifinis skydliaukės karcinomų žymuo yra padidėjęs tireoglobulino kiekis kraujyje. Tačiau jo nustatymo metodas ne visur prieinamas (meduliarinės karcinomos atveju toks žymuo yra didelis kalcitonino kiekis kraujyje). Esant techniniams sunkumams, galima rekomenduoti diagnostinį gydymą gliukokortikoidais: poveikio nebuvimas per 2 savaites vartojant 40–60 mg prednizolono per parą kalba prieš uždegiminę sankaupos liaukoje kilmę, pacientui nurodoma punkcijos biopsija.
Su kuo susisiekti?
Gydymas poūmis de Kvereno tiroiditas.
Poūmio tiroidito gydymas yra konservatyvus. Antibiotikų skyrimas patogenetiškai nepagrįstas. Greičiausias poveikis pasiekiamas skiriant gliukokortikoidus jų optimalaus priešuždegiminio poveikio dozėmis: 30–40 mg prednizolono per parą. Gydymo trukmė nustatoma pagal laiką, per kurį normalizuojasi ESR ir pašalinamas skausmo sindromas. Kaip parodė praktika, vaisto skyrimas kas antrą dieną yra mažiau veiksmingas, o santykinai trumpas gydymo kursas (1,5–2 mėnesiai) nesutrikdo normalaus santykio tarp paciento hipofizės ir antinksčių, o palaipsniui nutraukiant vaisto vartojimą, antinksčių nepakankamumo apraiškų nepastebėta. Gliukokortikoidų dozės mažinamos kontroliuojant ESR. Jei jis pagreitėja, būtina grįžti prie ankstesnės dozės. Vietoj gliukokortikoidų skiriami salicilo arba pirazolidono vaistai. Jų vartojimas kartu su gliukokortikoidais nėra pateisinamas, nes šių medžiagų opas sukeliantis poveikis skrandžio gleivinei yra sumuojamas, o gliukokortikoidų priešuždegiminis poveikis yra didesnis nei salicilatų. Merkazolilo vartojimas hipertiroidinėje fazėje yra netinkamas, nes tirotoksikozę sukelia pagreitėjęs anksčiau susintetintų hormonų patekimas į kraują, o merkazolilas sumažina jų susidarymą.
Rekomenduojama skirti beta adrenoblokatorių, kurie šalina tachikardiją ir skatina periferinį T4 virsmą į neaktyvią, atvirkštinę T3 formą. Beta adrenoblokatorių dozė paprastai svyruoja nuo 40 iki 120 mg/parą, gydymo trukmė – apie mėnesį. Skydliaukės hormonų skyrimas, kai sumažėja jų kiekis kraujyje, nurodomas tik esant ryškiems hipotirozės klinikiniams simptomams, paros dozė paprastai neviršija 0,1 g tiroidino, gydymo trukmė – 3–4 savaitės.
Liga linkusi kartotis, o gliukokortikoidų gydymo trukmė kartais siekia 4–6 mėnesius. Tokiu atveju pacientams gali pasireikšti gliukokortikoidų perdozavimo simptomai: svorio padidėjimas, veido apvalėjimas, strijos, padidėjęs kraujospūdis, hiperglikemija. Jei gliukokortikoidų terapijos nepavyksta nutraukti per 6–8 mėnesius, nurodomas chirurginis gydymas – atitinkamos liaukos skilties rezekcija.
Terapija gali būti atliekama vien salicilatais, kurių dozė yra 2,5–3 g/d. Tačiau poveikis pasiekiamas lėčiau nei vartojant gliukokortikoidus. Būtina salicilatų vartojimo sąlyga – jų tolygus pasiskirstymas per visą dieną.
Jei rezultatas teigiamas, gliukokortikoidų dozė sumažinama iki minimalios palaikomosios dozės (paprastai 10 mg prednizolono per parą), tada pridedama naprozino, aspirino arba reopirino, o prednizolono dozė sumažinama iki 1/2 tabletės kas tris dienas.
Prognozė
Poūmio de Quervain tiroidito prognozė yra palanki. Pacientų darbingumas paprastai atsistato per 1,5–2 mėnesius. Ambulatorinis stebėjimas 2 metus nuo ligos pradžios.

